CDP-Cholin (Cytisin-Diphosphat-Cholin, auch Citicolin) ist ein Nukleosiddiphosphat mit der Base Cytosin, das über einen Phosphorsäureester mit Cholin verknüpft ist. CDP-Cholin ist wasserlöslich und besitzt eine sehr gute Bioverfügbarkeit (> 90 %).
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
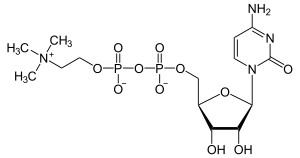
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Citicolin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C14H26N4O11P2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 487,32 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Wirkung im Körper
BearbeitenCDP-Cholin ist ein Zwischenprodukt des Zellmembranstoffwechsels, der als essentieller Baustein für die Biosynthese von Zellmembran-Phospholipiden (Phosphatidylcholin, auch: Lecithin) benötigt wird. CDP-Cholin wird endogen synthetisiert und stellt den limitierenden Schritt der Phosphatidylcholin-Synthese dar, dem wichtigsten Stoffwechselschritt zum Aufbau und zur Reparatur von Zellmembranen.
Pharmakokinetische Studien an gesunden Erwachsenen zeigten, dass oral appliziertes CDP-Cholin sehr schnell absorbiert und weniger als 1 % enteral ausgeschieden wird.[3][4] Exogen appliziertes CDP-Cholin wird in der Darmwand und in der Leber hydrolysiert und als Cholin und Cytidin absorbiert. Cholin und Cytidin werden dann weiter verstoffwechselt, passieren u. a. die Blut-Hirn-Schranke, um im Gehirn in CDP-Cholin resynthetisiert zu werden.[5] Pharmakokinetische Studien zeigen, dass die Ausscheidung respiratorisch über die Lunge sowie über den Urin analog zur Plasmaverfügbarkeit biphasisch verläuft.[6]
Cytidin, ein wichtiger Bestandteil von Nukleinsäuren (DNA/RNA), wird zytoplasmatisch in Cytidintriphosphat (CTP) umgewandelt. Im CDP-Cholin-Stoffwechsel wird Cholin durch das Enzym Cholin-Kinase phosphorylisiert. In der nachfolgenden Reaktion wird das Produkt Phosphorylcholin durch das Enzym CTP-Phosphocholin-Cytidintransferase (CCT) mit CTP unter Abspaltung einer Pyrophosphatgruppe zu CDP-Cholin umgesetzt.[7] Im letzten Schritt, katalysiert durch das Enzym Cholin-Phosphotransferase, reagiert CDP-Cholin mit Diacylglycerol zu Phosphatidylcholin.[8]
Im Tierversuch zeigte sich nach einer Behandlung mit 500 mg/kg KG/Tag über 90 Tage ein Anstieg der Phosphatidylcholin-Spiegel um 25 %, der Phosphatidylethanolamin-Spiegel um 17 % und der Phosphatidylserin-Spiegel um 42 %.[9] Cholin und Cytidin, die Hauptmetaboliten von CDP-Cholin, können bereits nach einer oralen Einmalgabe von CDP-Cholin durch signifikant erhöhte Plasmaspiegel bei jungen und älteren Patienten nachgewiesen werden. Durch MR-spektroskopische Untersuchungen konnte gezeigt werden, dass eine Behandlung mit CDP-Cholin über Wochen bei älteren Menschen die Plasmaspiegel von Phosphodiestern, Nebenprodukten des Phospholipid-Stoffwechsels, im Gehirn signifikant ansteigen lässt. Eine CDP-Cholin Behandlung erhöht somit die Phospholipid-Synthese sowie den Turnover.[10] CDP-Cholin hat sich in toxikologischen Tests als sehr sicher erwiesen, zeigte keine bedeutenden systemischen cholinergen Effekte.[11]
Einsatzgebiete
BearbeitenAufgrund seiner Wirkungsweise wurde CDP-Cholin schon früh mit regenerativen Funktionen bei traumatischen und degenerativen Hirnerkrankungen in Zusammenhang gebracht. Exogen zugeführtes CDP-Cholin wurde bei mehr als 11.000 Patienten in klinischen Studien untersucht (Schlaganfall, Schädel-Hirn-Trauma, Demenz). Besonders gut entschlüsselt sind die Wirkungen von CDP-Cholin nach einem (ischämischen oder hämorrhagischen) Schlaganfall: Beschrieben sind anti-exzitatorische, anti-oxidative, membran-stabilisierende und regenerative Wirkungen.[12] In klinischen Studien zeigten sich erste Hinweise auf eine Verkleinerung des Infarktvolumens sowie des neurologischen Defizites nach CDP-Cholin-Behandlung bei Schlaganfallpatienten.[3] So ergab eine Pooled-Data-Analyse zur Wirksamkeit von CDP-Cholin bei Patienten mit akutem ischämischem Schlaganfall, dass mehr als jeder vierte mit CDP-Cholin behandelte Patient nach drei Monaten eine weitgehend vollständige Wiederherstellung zeigte (NIHSS-Wert ≤ 1, Barthel-Index ≥ 95 plus mRS-Wert ≤ 1). Zudem bestätigt ein Cochrane-Review der gepoolten Daten aller sieben doppelblinder und placebokontrollierter Studien zum ischämischen Schlaganfall die Wirksamkeit von CDP-Cholin. Die Wahrscheinlichkeit für die Vermeidung von Mortalität/Behinderung im Langzeit-Follow-up fiel deutlich zugunsten von CDP-Cholin aus.[13] Nicht zuletzt aufgrund dieser Daten wird CDP-Cholin seit über 30 Jahren weltweit zur Schlaganfallbehandlung verwendet v. a. in Europa, Lateinamerika und Asien. Nach strengen evidenzbasierten Kriterien fehlt allerdings bislang ein Wirkungsnachweis aus einer multizentrischen Phase-III-Studie, der jedoch in einer internationalen Phase-III-Studie (ICTUS; International Citicholin Trial in Acute Stroke) aktuell geführt wird. Diese Studie wurde 2011 abgebrochen, da sich keine signifikanten Unterschiede bei der Verbesserung der Krankheitssymptome in den beiden teilnehmenden Gruppen (Verum gegen Placebo) ergaben. Als Ergebnis der Studie wurde festgehalten, dass Citicolin bei der Behandlung leichter und mittlerer ischämischer Schlaganfälle wirkungslos ist.[14]
Als weitere Einsatzgebiete werden u. a. kognitive Störungen unterschiedlicher Genese diskutiert, z. B. Demenz, Morbus Parkinson, Drogenabhängigkeit, Alkoholismus, Amblyopie und Glaukom,[11] sowie als Schutz der Endothelzell-Membranen bei Komplikationen nach infektiösen Erkrankungen wie Sepsis oder zerebraler Malaria.[15]
CDP-Cholin ist in Deutschland als Nahrungsergänzungsmittel frei verfügbar.
Siehe auch
BearbeitenWeblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Eintrag zu Citicoline in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 28. November 2018. (Seite nicht mehr abrufbar)
- ↑ a b W. R. Schäbitz: CDP-Cholin zur Behandlung des Schlaganfalls. In: Psychopharmakologie. 3, 2009, S. 101–105.
- ↑ A. Davalos, J. Castillo, J. Alvarez-Sabin u. a.: Oral citicoline in acute ischemic stroke: an individual patient data pooling analysis of clinical trials. In: Stroke. 33, 2002, S. 2850–2857.
- ↑ A. M. Rao, J. F. Hatcher, R. J. Dempsey: CDP-choline: neuroprotection in transient forebrain ischemia of gerbils. In: J Neurosci Res. 58, 1999, S. 697–705.
- ↑ J. R. Dinsdale, G. K. Griffiths, C. Rowlands u. a.: Pharmacokinetics of 14C CDP-choline. In: Arzneimittelforschung. 33, 1983, S. 1066–1070.
- ↑ I. L. G-Coviella, R. J. Wurtman: Enhancement by cytidine of membrane phospholipid synthesis. In: J Neurochem. 59(1), 1992, S. 338–343.
- ↑ K. J. D’Orlando, B. W. Sandage Jr.: Citicoline (CDP-choline): mechanisms of action and effects in ischemic brain injury. In: Neurol Res. 17, 1995, S. 281–284.
- ↑ I. Lopez-Coviella, J. Agut, V. Savci u. a.: Evidence that 5’-cytidinediphosphocholine can affect brain phospholipid composition by increasing choline and cytidine plasma levels. In: J Neurochem. 65, 1995, S. 889–894.
- ↑ S. M. Babb, L. L. Wald, B. M. Cohen u. a.: Chronic citicoline increases phosphodiesters in the brains of healthy older subjects: an in vivo phosphorus magnetic resonance spectroscopy study. In. Psychopharmacology. (Berl)
- ↑ a b J. J. Secades, J. L. Lorenzo: Citicoline: pharmacological and clinical review, 2006 update. In: Methods Find Exp Clin Pharmacol. 28(Suppl B), 2006, S. 1–56.
- ↑ W. R. Schäbitz u. a.: The effects of prolonged treatment with citicoline in temporary experimental focal ischemia. In: J Neurol Sci. 138, 1996, S. 21–25.
- ↑ J. L. Saver: 27th ISC, San Antonio, Texas 2002.
- ↑ A. Dávalos u. a.: Citicoline in the treatment of acute ischaemic stroke: an international, randomised, multicentre, placebo-controlled study (ICTUS trial). In: The Lancet. 380(9839), 28. Jul 2012, S. 349–357. doi:10.1016/S0140-6736(12)60813-7.
- ↑ R. Jambou, F. El-Assaad, V. Combes, G. E. Grau: Citicoline (CDP-choline): What role in the treatment of complications of infectious diseases. In. Int J Biochem Cell Biol. 1(7), 2009, S. 1467–1470. Epub 23. Februar 2009.