Fenobarbital
El fenobarbital o fenobarbitona es un barbitúrico, fabricado por primera vez por Bayer. La OMS lo recomienda para tratar ciertos tipos de epilepsia en países en desarrollo.[1] En el mundo desarrollado se usa comúnmente para tratar convulsiones en niños pequeños,[2] mientras que en niños mayores y adultos se usan otros fármacos.[3] Se puede administrar intravenosa, intramuscular y oralmente. Las formas inyectables se pueden usar para tratar crisis epilépticas. El fenobarbital es usado ocasionalmente para tratar problemas para dormir, ansiedad, síndrome de abstinencia y para ayudar en cirugías. Usualmente comienza a trabajar dentro de los cinco minutos de administrada vía intravenosa y media hora vía oral. Sus efectos duran entre cuatro y 48 horas.[4][5]
| Fenobarbital | ||
|---|---|---|
 | ||
 | ||
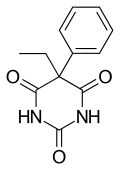
| Nombre (IUPAC) sistemático | ||
| 5-etil-5-fenil-1,3-diazinano-2,4,6-triona | ||
| Identificadores | ||
| Número CAS | 50-06-6 | |
| Código ATC | N05CA24 N03AA02 | |
| PubChem | 4763 | |
| DrugBank | APRD00184 | |
| Datos químicos | ||
| Fórmula | C12H12N2O3 | |
| Peso mol. | 232,235 g/mol | |
| Farmacocinética | ||
| Biodisponibilidad | >95% | |
| Metabolismo | Hepático (mayoritariamente CYP2C19) | |
| Vida media | 53-118 horas | |
| Excreción | Renal y fecal | |
| Datos clínicos | ||
| Nombre comercial | Luminal® | |
| Cat. embarazo | Evidencia de riesgo para el feto, aunque el beneficio potencial de su uso en embarazadas puede ser aceptable a pesar del riesgo probable solo en algunas situaciones. Queda a criterio del médico tratante. (EUA) | |
| Vías de adm. | Oral, rectal, parenteral (intramuscular e intravenosa) | |
Los efectos secundarios pueden incluir la disminución del nivel de conciencia junto con la disminución de la fuerza para respirar. Hay preocupación acerca del abuso de esta sustancia así como también sobre su retiro luego de un uso a largo plazo. También puede incrementar el riesgo de suicidio. En EE. UU. es categoría B o D para mujeres embarazadas, dependiendo cómo se tome y categoría D en Australia, lo que significa que puede causar daños. Si se usa durante el amamantamiento puede darle mareos al bebé. Se recomiendan dosis más bajas para personas con funciones renales o hepáticas empobrecidas y en personas mayores.
El fenobarbital tiene propiedades sedantes e hipnóticas, pero al igual que pasa con el resto de barbitúricos, en este aspecto se usan más las benzodiacepinas. Aumenta la actividad de los neurotransmisores inhibitorios GABA. Fue descubierto en 1912 y es el anticonvulsivo más antiguo que aún se utiliza en la actualidad y el más barato, de un costo de alrededor de cinco dólares al año en los países en desarrollo. Sin embargo, el acceso se puede dificultar en aquellos países que lo clasifican como droga controlada.
Figura en la lista de medicamentos esenciales de la OMS,[6] lista que enumera los medicamentos más efectivos y seguros para un sistema básico de atención sanitaria. En países más desarrollados, no es el medicamento de primera elección para la mayoría de los ataques convulsivos,[7][8] aunque se usa bastante en casos de convulsiones neonatales.[9]
Historia
editarEl primer barbitúrico, el barbital, fue sintetizado en 1902 por los químicos alemanes Emil Fisher y Josef von Mering en Bayer. En 1904, Fisher sintetizó algunos compuestos parecidos, entre ellos el fenobarbital. Este fue comercializado por primera vez en 1912, bajo la marca comercial Luminal. Se usó como sedante e hipnótico hasta 1950, cuando aparecieron las benzodiacepinas.[10]
Entre 1934 y 1945 el fenobarbital fue usado por los médicos alemanes de la Alemania nazi para matar a los niños que nacían enfermos o con deformidades físicas, dentro del programa de eugenesia que había puesto en marcha el Partido Nazi. La Operación T-4, dentro de la cual fueron asesinados todos aquellos niños que no cumplían el "estándar" ario, fue un precursor del Holocausto, y gran cantidad de personal médico que estuvo implicado en este programa fue luego transferido a los campos de concentración nazis, donde pusieron en práctica todo el saber hacer que habían aprendido anteriormente.[11] [12]
Las propiedades hipnóticas, sedantes y soporíferas del fenobarbital eran conocidas en 1912, pero en ese momento nadie sabía que tenía además propiedades anticonvulsivas. El doctor Alfred Hauptmann lo usó en una ocasión como tranquilizante en pacientes con convulsiones, y al ver que éstas remitían, emprendió un largo estudio con este tipo de pacientes. Muchos de los pacientes de Hauptmann estaban siendo tratados con bromuro de potasio, el único medicamento efectivo en ese momento, pero este tenía desagradables efectos secundarios y una eficacia limitada. Cuando les fue administrado el fenobarbital, la frecuencia y la intensidad de los ataques disminuyó, y aquellos que sólo tenían ataques no demasiado importantes se libraron de ellos. Además, mejoró su salud física y mental al retirar el bromuro de potasio de su tratamiento. Aquellos pacientes que estaban internos en centros de salud debido a la severidad de su epilepsia fueron capaces de volver a sus casas, y en algunos casos, volver al trabajo. Resultó que el fenobarbital no era una cura para la epilepsia; la retirada del medicamento llevaba a los pacientes a sufrir ataques con una mayor frecuencia. El fenobarbital fue ampliamente acogido como el primer medicamento anticonvulsivo realmente efectivo, aunque la Primera Guerra Mundial retrasó su introducción en EE. UU.[13]
Se usó como tratamiento para la ictericia neonatal, al aumentar la tasa metabólica del hígado y por consiguiente disminuir los niveles de bilirrubina. En la década de 1950 se descubrió la fototerapia, y se convirtió en el tratamiento estándar.[14]
En 1940, Winthrop Chemical fabricó pastillas de sulfatiazol contaminadas con fenobarbital. Esto ocurrió porque ambos medicamentos se fabricaron a la vez y en paralelo y posiblemente algunas herramientas fueron intercambiadas. Cada pastilla de sulfatiazol incluyó más del doble de la cantidad de fenobarbital necesario para inducir el sueño. Centenares de pacientes murieron o resultaron afectados. Una investigación de la FDA estadounidense culpó directamente a Winthrop y como resultado se introdujeron las Buenas prácticas de manufactura.[14]
El fenobarbital se usó durante más de 25 años como tratamiento profiláctico de las convulsiones febriles.[15] Aunque es un tratamiento efectivo y el paciente no corre el riesgo de desarrollar epilepsia, dicho uso no está recomendado actualmente.[16][17]
Mecanismo de acción
editarInhibe las convulsiones mediante la potenciación (agonismo) del receptor GABAA causando inhibición sináptica. El fenobarbital se une a la subunidad β del receptor causando apertura del canal, aumento de la conductancia gCl- y subsecuente entrada de Cl- llevando el voltaje transmembranal hacia el potencial de equilibrio del cloro (-70 mV) estabilizando la célula y reduciendo la probabilidad de una generación de potencial de acción por estímulos excitatorios.[18]
Análisis en ratones han mostrado que el fenobarbital incrementa la corriente mediaba por GABAA al incrementar la duración de la corriente sin cambiar la frecuencia de la misma.[19]
Indicaciones
editarEl fenobarbital se usa en el tratamiento de todo tipo de convulsiones, excepto las de ausencia.[7][20] No es menos efectivo que otros medicamentos modernos como la fenitoína y la carbamazepina, pero se tolera peor.[21][22]
En el tratamiento del status epiléptico se usa, como primera opción, benzodiacepinas de acción rápida como el diazepam o el lorazepam. Si éstos fallan, se recurre a la fenitoína, con el fenobarbital como alternativa (en EE. UU. y el Reino Unido este fármaco se usa como tercera alternativa).[23] Si todos los medicamentos anteriores fallan, se recurre a la anestesia y a cuidados intensivos.[20][24]
Sí se usa, como primera opción, en los casos de convulsiones neonatales.[9][25][26] Los temores a que dichas convulsiones sean perjudiciales hacen que los médicos las traten de una manera agresiva, aunque no hay evidencias de lo primero.[27]
Efectos secundarios
editarLos principales efectos secundarios son la sedación y la osteoporosis, efectos que se pueden contrarrestar, la sedación con 1-2 horas más de sueño y la osteoporosis, ya que modifica la absorción de vitamina D. En pacientes de edad avanzada, también se ha observado excitación y confusión, mientras que los niños pueden sufrir hiperactividad paradójica (poco probable).
Contraindicaciones
editarEl fenobarbital está contraindicado en la porfiria aguda intermitente, hipersensibilidad a los barbitúricos, insuficiencia respiratoria grave, dependencia a los barbitúricos en etapas anteriores e hiperquinesia infantil y es muy tóxico en combinación con ácido valproico, (en cualquiera de sus sales), ya que entre otras cosas, produce aumento de crisis, en lugar de disminuirlas, y está indicado aumento de dosis de medicamento, siendo esto, (el aumento) totalmente contraproducente, aquí lo que hay que hacer es eliminar el ácido valproico del organismo y no dar fenobarbital hasta 6-8 después, ya que se elimine el ácido valproico del organismo, aumentar la hidratación para acelerar la eliminación del ácido valproico, eliminando con esto la intoxicación medicamentosa
Sobredosis
editarEl fenobarbital "deprime" los sistemas del cuerpo, principalmente los sistemas nerviosos central y periférico; la principal característica de una sobredosis de fenobarbital es una ralentización de las funciones corporales, incluyendo conciencia alterada (incluso coma), bradicardia, bradipnea, hipotermia e hipotensión. También puede provocar edema pulmonar y fallo renal agudo, a consecuencia del shock.
El electroencefalograma de una persona con sobredosis de fenobarbital presenta actividad eléctrica disminuida, hasta el punto de parecer muerte cerebral. Esto es debido a la profunda depresión del sistema nervioso central que provoca el medicamento, aunque dicha depresión es reversible.[28]
El tratamiento de dicha sobredosis es de soporte, e incluye mantener abierta la vía aérea (incluyendo intubación endotraqueal y ventilación asistida), corrección de la bradicardia (incluyendo los líquidos intravenosos y los vasopresores) y la eliminación de la mayor cantidad posible de medicamento del cuerpo. Dependiendo de la dosis ingerida y del tiempo transcurrido desde la ingestión, dicha eliminación puede hacerse vía lavado gástrico o administración de carbón activado. La hemodiálisis también es efectiva, y puede reducir la vida media de eliminación hasta en un 90 %.[28] No hay un antídoto específico para el envenenamiento por fenobarbital.
Farmacocinética
editarEl fenobarbital tiene una biodisponibilidad oral de un 90 %. El pico de concentración plasmática llega a las 8-12 horas después de la administración oral. Es uno de los barbitúricos de acción más prolongada, con una vida media de eliminación de 70 a 120 horas, (3 a 5 días) y su grado de unión a las proteínas plasmáticas es bajo, de un 20 a un 45 %. Se metaboliza principalmente en el hígado, principalmente vía hidroxilación y glucuronodización, e implica a muchas isozimas del sistema citocromo P-450 oxidasa, principalmente la CYP2C9 y en menor grado CYP2C19 y CYP2E1. También implica al sistema citocromo P450 2B6. Se excreta vía renal.
Interacciones farmacológicas
editarSus interacciones comprenden la inducción de enzimas citocromos P450 hepáticos. Administrado junto con ácido valproico aumenta las concentraciones plasmáticas de fenobarbital hasta en un 40 %.
Uso veterinario
editarEl fenobarbital se usa para tratar la epilepsia canina, además de la felina.[29]
También se puede usar para tratar las convulsiones en los caballos cuando el tratamiento con benzodiazepinas falla o está contraindicado.[30]
Referencias
editar- Ole Daniel Enersen. «Alfred Hauptmann». Consultado el 2006-09-06.
- Kwan P, Brodie M (2004). «Phenobarbital for the treatment of epilepsy in the 21st century: a critical review.». Epilepsia 45 (9): 1141-9. PMID 15329080. Archivado desde el original el 16 de diciembre de 2018. Consultado el 10 de abril de 2007.
Notas
editar- ↑ Ilangaratne, NB; Mannakkara, NN; Bell, GS; Sander, JW (1 de diciembre de 2012). «Phenobarbital: missing in action.». Bulletin of the World Health Organization 90 (12): 871-871A. PMC 3524964. PMID 23284189. doi:10.2471/BLT.12.113183.
- ↑ Brodie, MJ; Kwan, P (Diciembre de 2012). «Current position of phenobarbital in epilepsy and its future.». Epilepsia. 53 Suppl 8: 40-6. PMID 23205961. doi:10.1111/epi.12027.
- ↑ «The epilepsies: the diagnosis and management of the epilepsies in adults and children in primary and secondary care NICE guidelines [CG137]». National Institute for Health and Care Excellence. Enero de 2012.
- ↑ Bassert, Joanna M. (2017). McCurnin's Clinical Textbook for Veterinary Technicians - E-Book (en inglés). Elsevier Health Sciences. p. 955. ISBN 9780323496407.
- ↑ «Phenobarbital». The American Society of Health-System Pharmacists. Archivado desde el original el 6 de septiembre de 2015. Consultado el 16 de diciembre de 2018.
- ↑ «WHO Model List of Essential Medicines» (PDF). World Health Organization. March 2005. Archivado desde el original el 12 de febrero de 2007. Consultado el 12 de marzo de 2006.
- ↑ a b NICE (2005-10-27). «CG20 Epilepsy in adults and children: NICE guideline». NHS. Archivado desde el original el 9 de octubre de 2006. Consultado el 6 de septiembre de 2006.
- ↑ «Phenobarbital». Epilepsy Foundation. Consultado el 7 de septiembre de 2006.
- ↑ a b British Medical Association, Royal Pharmaceutical Society of Great Britain, Royal College of Paediatrics and Child Health and Neonatal and Paediatric Pharmacists Group (2006). «4.8.1 Control of epilepsy». British National Formulary for Children. pp. 255-6. ISBN 0-85369-676-4.
- ↑ Sneader, Walter (23 de junio de 2005). Drug Discovery. John Wiley and Sons. pp. 369. ISBN 0-471-89979-8. Consultado el 6 de septiembre de 2006.
- ↑ Marylynne Pitz (2006-12-20). «A Warhol show explores Germany's Master Race philosophy». Post-Gazette. PG Publishing Co., Inc. Consultado el 20 de marzo de 2007.
- ↑ Naomi Schaefer (marzo de 2004). «The Legacy of Nazi Medicine». The New Atlantis, Number 5. pp. 54-60. Archivado desde el original el 7 de septiembre de 2008. Consultado el 20 de marzo de 2007.
- ↑ Scott,, Donald F (1993-02-15). The History of Epileptic Therapy. Taylor & Francis. pp. 59-65. ISBN 1-85070-391-4.
- ↑ a b Rachel Sheremeta Pepling (06 de 2005). «Phenobarbital». Chemical and Engineering News 83 (25). Consultado el 6 de septiembre de 2006.
- ↑ John M. Pellock, W. Edwin Dodson, Blaise F. D. Bourgeois (2001-01-01). Pediatric Epilepsy. Demos Medical Publishing. p. 169. ISBN 1-888799-30-7.
- ↑ Robert Baumann (2005-02-14). «Febrile Seizures». eMedicine. WebMD. Consultado el 6 de septiembre de 2006.
- ↑ various (marzo de 2005). «Diagnosis and management of epilepsies in children and young people». Scottish Intercollegiate Guidelines Network. p. 15. Archivado desde el original el 10 de junio de 2006. Consultado el 7 de septiembre de 2006.
- ↑ E.,, Golan, David; J.,, Armstrong, Ehrin; W.,, Armstrong, April; Germán,, Arias Rebatet,. Principios de Farmacología : bases fisiopatológ̤icas del tratamiento farmacológ̤ico (Cuarta edición edición). ISBN 9788416781003. OCLC 950446093.
- ↑ L., Brunton, Laurence; Bruce., Chabner,; C., Knollmann, Björn (2012). Goodman & Gilman las bases farmacológicas de la terapéutica (12 ed edición). McGrawHill. ISBN 9786071506412. OCLC 970512384.
- ↑ a b British National Formulary 51
- ↑ Taylor S, Tudur Smith C, Williamson PR, Marson AG (2003). «Phenobarbitone versus phenytoin monotherapy for partial onset seizures and generalized onset tonic-clonic seizures.». Cochrane Database Systematic Reviews (2). doi:10.1002/14651858.CD002217. PMID 11687150. Archivado desde el original el 16 de junio de 2020. Consultado el 6 de septiembre de 2006.
- ↑ Tudur Smith C, Marson AG, Williamson PR (2003). «Carbamazepine versus phenobarbitone monotherapy for epilepsy». Cochrane Database of Systematic Reviews (1). doi:10.1002/14651858.CD001904. PMID 12535420. Archivado desde el original el 16 de junio de 2020. Consultado el 6 de septiembre de 2006.
- ↑ British Medical Association, Royal Pharmaceutical Society of Great Britain, Royal College of Paediatrics and Child Health and Neonatal and Paediatric Pharmacists Group (2006). «4.8.2 Drugs used in status epilepticus». British National Formulary for Children. pp. 269. ISBN 0-85369-676-4.
- ↑ Kälviäinen R, Eriksson K, Parviainen I (2005). «Refractory generalised convulsive status epilepticus : a guide to treatment.». CNS Drugs 19 (9): 759-68. PMID 16142991.
- ↑ John M. Pellock, W. Edwin Dodson, Blaise F. D. Bourgeois (2001-01-01). Pediatric Epilepsy. Demos Medical Publishing. p. 152. ISBN 1-888799-30-7.
- ↑ Raj D Sheth (2005-03-30). «Neonatal Seizures». eMedicine. WebMD. Consultado el 6 de septiembre de 2006.
- ↑ Booth D, Evans DJ (2004). «Anticonvulsants for neonates with seizures». Cochrane Database of Systematic Reviews (3). doi:10.1002/14651858.CD004218.pub2. PMID 15495087. Archivado desde el original el 16 de junio de 2020. Consultado el 6 de septiembre de 2006.
- ↑ a b Rania Habal (2006-01-27). «Barbiturate Toxicity». eMedicine. WebMD. Consultado el 14 de septiembre de 2006.
- ↑ Thomas, WB (2003). Seizures and narcolepsy. In: Dewey, Curtis W. (ed.) A Practical Guide to Canine and Feline Neurology. Ames, Iowa: Iowa State Press. ISBN 0-8138-1249-6.
- ↑ Kahn, Cynthia M., Line, Scott, Aiello, Susan E. (ed.), ed. (8 de febrero de 2005). The Merck Veterinary Manual (9th ed. edición). John Wiley & Sons. ISBN 0-911910-50-6.