Diferencia entre revisiones de «Cianohidrina»
m r2.5.2) (robot Añadido: fi:Syanohydriinit |
Deshecha la edición 162364495 de UA31 (disc.) Como ya dije en otro artículo, Aimep3 no es relevante aquí. Etiqueta: Deshecho |
||
| (No se muestran 15 ediciones intermedias de 13 usuarios) | |||
| Línea 1: | Línea 1: | ||
[[Archivo:Cyanohydrin-general-2D-skeletal.png| |
[[Archivo:Cyanohydrin-general-2D-skeletal.png|miniaturadeimagen|Estructura general de una cianohidrina.]] |
||
En [[química orgánica]], una '''cianohidrina''', también llamada '''cianhidrina''', es un [[grupo funcional]] encontrado en [[compuesto orgánico|compuestos orgánicos]]. Las cianohidrinas tienen la fórmula R<sub>2</sub>C(OH)CN, donde R es [[hidrógeno|H]], [[alquilo]], o [[arilo]]. Las cianohidrinas son importantes precursores industriales de los [[ácido carboxílico|ácidos carboxílicos]] y algunos [[aminoácido]]s. Las cianohidrinas pueden ser formadas por la [[reacción de cianohidrina]], que involucra el tratamiento de una [[Cetona (química)|cetona]] o un [[aldehído]] con [[cianuro de hidrógeno]] (HCN), |
En [[química orgánica]], una '''cianohidrina''', también llamada '''cianhidrina''', es un [[grupo funcional]] encontrado en [[compuesto orgánico|compuestos orgánicos]]. Las cianohidrinas tienen la fórmula R<sub>2</sub>C(OH)CN, donde R es [[hidrógeno|H]], [[alquilo]], o [[hidrocarburo aromático|arilo]]. Las cianohidrinas son importantes precursores industriales de los [[ácido carboxílico|ácidos carboxílicos]] y algunos [[aminoácido]]s. Las cianohidrinas pueden ser formadas por la [[reacción de cianohidrina]], que involucra el tratamiento de una [[Cetona (química)|cetona]] o un [[aldehído]] con [[cianuro de hidrógeno]] (HCN), con [[cianuro de sodio]] (NaCN) como catalizador: |
||
:RR’C=O + HCN → RR’C(OH)CN |
:RR’C=O + HCN → RR’C(OH)CN |
||
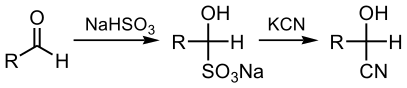
En esta reacción, el ion [[nucleófilo]] CN<sup>−</sup> ataca al carbono [[electrófilo]] del carbonilo en la cetona, seguido por la protonación por el HCN, con lo que se regenera el anión cianuro. Las cianohidrinas también son preparadas por desplazamiento de [[sulfito]] por sales de cianuro:<ref name=Corson>{{OrgSynth | author = Corson, B. B.; Dodge, R. A.; Harris, S. A.; Yeaw, J. S. | title = Mandelic Acid | collvol = 1 | collvolpages = 336 | year = 1941 | prep = cv1p0336}}</ref> |
En esta reacción, el ion [[nucleófilo]] CN<sup>−</sup> ataca al carbono [[electrófilo]] del carbonilo en la cetona, seguido por la [[protonación]] por el HCN, con lo que se regenera el [[anión]] cianuro. Las cianohidrinas también son preparadas por desplazamiento de [[sulfito]] por sales de cianuro:<ref name=Corson>{{OrgSynth | author = Corson, B. B.; Dodge, R. A.; Harris, S. A.; Yeaw, J. S. | title = Mandelic Acid | collvol = 1 | collvolpages = 336 | year = 1941 | prep = cv1p0336}}</ref> |
||
[[Archivo:Cyanation of aldehyde with bisulfate.svg| |
[[Archivo:Cyanation of aldehyde with bisulfate.svg|407x407px|Cianuración de aldehído con bisulfato]] |
||
Las cianohidrinas son intermediarios en la [[síntesis de aminoácidos de Strecker]]. |
Las cianohidrinas son intermediarios en la [[síntesis de aminoácidos de Strecker]]. |
||
== Cianohidrinas de acetona == |
== Cianohidrinas de acetona == |
||
La [[cianohidrina de acetona]], (CH<sub>3</sub>)<sub>2</sub>C(OH)CN, es generada como un intermediario en la producción industrial del [[metacrilato de metilo]].<ref>William Bauer, Jr. "Methacrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441. Article Online Posting Date: June 15, 2000</ref> En el laboratorio, este líquido sirve como una fuente de HCN, que es inconvenientemente volátil.<ref>Haroutounian, S. A. ”Acetone Cyanohydrin” Encyclopedia of Reagents for Organic Synthesis 2001, John Wiley & Sons. DOI: 10.1002/047084289X.ra014</ref> En consecuencia, la cianohidrina de acetona puede ser utilizada para la preparación de otras cianohidrinas, para liberar HCN a los [[adición de Michael|aceptores de Michael]], y para la [[reacción de Gattermann-Koch|formilación]] de [[areno]]s. El tratamiento de esta cianohidrina con [[hidruro de litio]] produce el cianuro de litio anhidro: |
La [[cianohidrina de acetona]], (CH<sub>3</sub>)<sub>2</sub>C(OH)CN, es generada como un intermediario en la producción industrial del [[metacrilato de metilo]].<ref>William Bauer, Jr. "Methacrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441. Article Online Posting Date: June 15, 2000</ref> En el laboratorio, este líquido sirve como una fuente de HCN, que es inconvenientemente volátil.<ref>Haroutounian, S. A. ”Acetone Cyanohydrin” Encyclopedia of Reagents for Organic Synthesis 2001, John Wiley & Sons. DOI: 10.1002/047084289X.ra014</ref> En consecuencia, la cianohidrina de [[acetona]] puede ser utilizada para la preparación de otras cianohidrinas, para liberar HCN a los [[adición de Michael|aceptores de Michael]], y para la [[reacción de Gattermann-Koch|formilación]] de [[areno]]s. El tratamiento de esta cianohidrina con [[hidruro de litio]] produce el cianuro de litio anhidro: |
||
:[[Archivo:LiCN-from-acetone-cyanohydrin-2D-skeletal.png| |
:[[Archivo:LiCN-from-acetone-cyanohydrin-2D-skeletal.png|453x453px]] |
||
== Otras cianohidrinas == |
== Otras cianohidrinas == |
||
| Línea 22: | Línea 22: | ||
<center> |
<center> |
||
{|align="center" class="wikitable" |
{|align="center" class="wikitable" |
||
|<center>[[Archivo: |
|<center>[[Archivo:Glyconitrile Structural FormulaV1.svg|100px]]</center>||<center>[[Archivo:Acetone cyanohydrin.svg|100px]]</center>||<center>[[Archivo:Mandelonitrile-2D-skeletal.svg|100px]]</center> |
||
|- |
|- |
||
|<center>glicolonitrilo</center>||<center>cianohidrina de la acetona</center>||<center>mandelonitrilo</center> |
|<center>glicolonitrilo</center>||<center>cianohidrina de la acetona</center>||<center>mandelonitrilo</center> |
||
| Línea 32: | Línea 32: | ||
== Enlaces externos == |
== Enlaces externos == |
||
* [[IUPAC]]s [[Gold Book]] definición de cianohidrinas [http://www.iupac.org/goldbook/C01489.pdf] |
* [[IUPAC]]s [[Gold Book]] definición de cianohidrinas [https://web.archive.org/web/20070610060228/http://www.iupac.org/goldbook/C01489.pdf] |
||
{{Control de autoridades}} |
|||
[[Categoría:Grupos funcionales]] |
[[Categoría:Grupos funcionales]] |
||
[[da:Cyanohydrin]] |
|||
[[de:Cyanhydrine]] |
|||
[[en:Cyanohydrin]] |
|||
[[fi:Syanohydriinit]] |
|||
[[fr:Cyanohydrine]] |
|||
[[it:Cianidrine]] |
|||
[[ja:シアノヒドリン]] |
|||
[[nl:Cyanohydrine]] |
|||
[[pl:Cyjanohydryny]] |
|||
[[ru:Циангидрины]] |
|||
[[zh:羟腈]] |
|||
Revisión actual - 20:43 10 sep 2024

En química orgánica, una cianohidrina, también llamada cianhidrina, es un grupo funcional encontrado en compuestos orgánicos. Las cianohidrinas tienen la fórmula R2C(OH)CN, donde R es H, alquilo, o arilo. Las cianohidrinas son importantes precursores industriales de los ácidos carboxílicos y algunos aminoácidos. Las cianohidrinas pueden ser formadas por la reacción de cianohidrina, que involucra el tratamiento de una cetona o un aldehído con cianuro de hidrógeno (HCN), con cianuro de sodio (NaCN) como catalizador:
- RR’C=O + HCN → RR’C(OH)CN
En esta reacción, el ion nucleófilo CN− ataca al carbono electrófilo del carbonilo en la cetona, seguido por la protonación por el HCN, con lo que se regenera el anión cianuro. Las cianohidrinas también son preparadas por desplazamiento de sulfito por sales de cianuro:[1]
Las cianohidrinas son intermediarios en la síntesis de aminoácidos de Strecker.
Cianohidrinas de acetona
[editar]La cianohidrina de acetona, (CH3)2C(OH)CN, es generada como un intermediario en la producción industrial del metacrilato de metilo.[2] En el laboratorio, este líquido sirve como una fuente de HCN, que es inconvenientemente volátil.[3] En consecuencia, la cianohidrina de acetona puede ser utilizada para la preparación de otras cianohidrinas, para liberar HCN a los aceptores de Michael, y para la formilación de arenos. El tratamiento de esta cianohidrina con hidruro de litio produce el cianuro de litio anhidro:
Otras cianohidrinas
[editar]El mandelonitrilo, con fórmula C6H5CH(OH)CN, está presente en pequeñas cantidades en algunas frutas.[1] Se conocen glicósidos cianogénicos relacionados, como la amigdalina.
El glicolonitrilo, también llamado hidroxiacetonitrilo o cianohidrina del formaldehído (CAS#107-16-4), es el compuesto orgánico con fórmula HOCH2CN. Es la cianohidrina más simple, derivando del formaldehído.[4]
 |
 |
 |
Referencias
[editar]- ↑ a b Corson, B. B.; Dodge, R. A.; Harris, S. A.; Yeaw, J. S. (1941). "Mandelic Acid". Org. Synth.; Coll. Vol. 1: 336.
- ↑ William Bauer, Jr. "Methacrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441. Article Online Posting Date: June 15, 2000
- ↑ Haroutounian, S. A. ”Acetone Cyanohydrin” Encyclopedia of Reagents for Organic Synthesis 2001, John Wiley & Sons. DOI: 10.1002/047084289X.ra014
- ↑ Gaudry, R. (1955). "Glycolonitrile". Org. Synth.; Coll. Vol. 3: 436.