Ontwikkeling van het hart

De ontwikkeling van het hart, ook wel cardiogenese genoemd, is de ontwikkeling van het hart tot de bevalling. Het begint met de vorming van twee endocardiale buizen die samensmelten tot het buisvormige hart, ook wel de primitieve of primaire hartbuis genoemd. De primitieve hartbuis bestaat uit drie lagen. Van binnen naar buiten zijn dit het endocard, de endocardgelei/hartgelei (cardiac jelly) en het myocard. Tegelijkertijd met de hartbuis ontstaat de pericardholte, dat de pompfunctie mogelijk maakt. Het hart is het eerste functionele orgaan in embryo's van gewervelden.
Het buisvormige hart differentieert snel in de truncus arteriosus, bulbus cordis, primitieve ventrikel, primitieve atrium en de sinus venosus (instroomkanaal). De truncus arteriosus verdeelt het bloed over de rest van het embryo en splitst zich in de opstijgende aorta en de longslagaderstam. De bulbus cordis vormt een deel van de ventrikels. De sinus venosus is verbonden met de foetale bloedsomloop.
De hartbuis wordt langer aan de rechterkant, vormt een lus en wordt het eerste visuele teken van links-rechtsasymmetrie van het lichaam. Scheidingswanden vormen zich in de boezems en ventrikels om de linker- en rechterkant van het hart te scheiden.[3]
Vroege ontwikkeling
[bewerken | brontekst bewerken]Het hart is afkomstig van embryonale mesodermale kiembladcellen die na gastrulatie differentiëren in mesotheel, endotheel en hartspierweefsel. Hartinductie vindt plaats in het voorste mesoderm tijdens gastrulatie door interacties met aangrenzend endoderm (zowel extra-embryonaal als definitief endoderm) voornamelijk met behulp van endogene remmers van Wnt-signalering zoals DKK1.[4][5] Het mesotheliaal pericardium vormt de buitenste bekleding van het hart. De binnenste bekleding van het hart – het endocard, lymfe- en bloedvaten, ontwikkelen zich vanuit het endotheel.[6][2]
Endocardiale buizen
[bewerken | brontekst bewerken]In het splanchnopleurale mesenchym aan beide kanten van de neurale plaat ontwikkelt zich een hoefijzervormig gebied als de cardiogene regio. Dit is gevormd uit hartspiercellen en bloedeilanden als voorlopers van bloedcellen en bloedvaten.[7] Op dag 19 na de bevruchting begint zich aan beide kanten van deze regio een endocardiale buis te ontwikkelen. Deze twee buizen zijn in de derde week naar elkaar toegegroeid om vervolgens samen te smelten, waarbij door geprogrammeerde celdood één buis wordt gevormd, het buisvormige hart.[8]
Vanuit het splanchnopleurale mesenchym ontwikkelt de cardiogene regio zich craniaal en lateraal ten opzichte van de neurale plaat. In dit gebied vormen zich aan beide kanten twee afzonderlijke angiogene celclusters die samensmelten tot de endocardiale buizen. Wanneer de embryonale vouwing begint, worden de twee endocardiale buizen in de borstholte geduwd, waar ze beginnen te fuseren. Na ongeveer 22 dagen na de bevruchting is de fusie voltooid.[9][2]
Ongeveer 18 tot 19 dagen na de bevruchting begint het hart zich te vormen. Het hart begint zich te ontwikkelen nabij het hoofd van het embryo in het cardiogene gebied.[1] Na celsignalering beginnen zich twee strengen of koorden te vormen in het cardiogene gebied.[1] Terwijl deze zich vormen, ontwikkelt zich er een lumen in, op welk punt ze endocardiale buizen worden genoemd.[1] Tegelijkertijd dat de buizen zich vormen, worden ook andere belangrijke hartcomponenten gevormd.[8] De twee buizen migreren samen en fuseren om een enkele primitieve hartbuis te vormen die snel vijf verschillende regio's vormt.[1] Van kop tot staart zijn dit de truncus arteriosus, bulbus cordis, primitieve ventrikel, primitieve atrium en de sinus venosus.[1] Aanvankelijk stroomt al het aderlijke bloed de sinus venosus in en samentrekkingen stuwen het bloed van staart naar kop, of van de sinus venosus naar de truncus arteriosus.[1] De truncus arteriosus zal zich splitsen en de aorta en de longslagader vormen; de bulbus cordis zal zich ontwikkelen tot het rechterventrikel; het primitieve ventrikel zal het linkerventrikel vormen; het primitieve atrium zal de voorste delen van de linker- en rechterboezem en hun aanhangsels worden en de sinus venosus zal zich ontwikkelen tot het achterste deel van het rechteratrium, de sinusknoop en de sinus coronarius.[1]
Positie van de hartbuis
[bewerken | brontekst bewerken]
Het centrale deel van het cardiogene gebied bevindt zich voor het orofaryngeale membraan en de neurale plaat. De groei van de hersenen en de hoofdplooien duwen het orofaryngeale membraan naar voren, terwijl het hart en de pericardiale holte eerst naar de halsregio en vervolgens naar de borstkas bewegen. Het gebogen deel van het hoefijzervormige gebied breidt zich uit om de toekomstige ventriculaire conus arteriosus (uitstroomkanaal) en de ventriculaire regio's te vormen, terwijl de hartbuis zich blijft uitbreiden. (De conus arteriosus is een conische formatie in het rechter ventrikel, uit wiens top de longslagader ontstaat.) De buis begint aderlijke drainage te krijgen in zijn caudale pool en zal bloed uit de eerste aortaboog en in de dorsale aorta pompen via zijn polaire hoofd. Aanvankelijk blijft de buis vastzitten aan het dorsale deel van de pericardiale holte door een mesodermale weefselplooi die het paraxiaal mesoderm wordt genoemd. Dit mesoderm verdwijnt om de twee pericardiale sinussen te vormen, de transversale en de scheve pericardiale sinussen, die beide zijden van de pericardiale holte verbinden.[7]
Het hartspierweefsel wordt dikker en scheidt een dikke laag van rijke extracellulaire matrix af die hyaluronzuur bevat, dat het endotheel scheidt. Vervolgens vormen mesotheelcellen het pericardium en migreren om het grootste deel van het epicardium te vormen. Vervolgens wordt de hartbuis gevormd door het endocardium, wat de binnenste endotheelbekleding van het hart is en de myocardiale spierwand, wat het epicardium is dat de buitenkant van de buis bedekt.[7]
Vouwen en draaien van het hart
[bewerken | brontekst bewerken]De hartbuis blijft zich uitrekken en op dag 23 na de bevruchting, in een proces dat morfogenese wordt genoemd, begint de hartlus. Het hoofddeel buigt in een frontale richting met de klok mee. Het atriale deel begint te bewegen in de richting van de hals en beweegt dan naar links vanaf zijn oorspronkelijke positie. Deze gebogen vorm nadert het hart en voltooit zijn groei op dag 28 na de bevruchting. De buis vormt de atriale en ventriculaire verbindingen die het gemeenschappelijke atrium en het gemeenschappelijke ventrikel verbinden in het vroege embryo. De arteriële bulb vormt het trabeculaire deel van het rechterventrikel. Een kegel zal het ventriculaire conus arteriosusbloed van beide ventrikels vormen. De arteriële stam en de zijtakken zullen het proximale deel van de aorta en de longslagader vormen. De verbinding tussen het ventrikel en de arteriële bulb wordt het primaire intraventriculaire gat genoemd. De buis is verdeeld in hartregio's langs zijn craniocaudale (van kop naar staart) as: het primitieve ventrikel, primitief linkerventrikel genoemd, en de trabeculaire proximale arteriële bulbus, primitief rechterventrikel genoemd.[10] Op dit moment is er in het hart geen tussenschot aanwezig .
Een functionele verklaring voor de draaiing van het hart en de darmen ontbreekt, maar één theorie geeft wel een verklaring voor de evolutie en ontwikkeling van dit fenomeen. Volgens deze axiale draaitheorie komt dit door een draaiing in het lichaam van alle gewervelde dieren die optreedt in het vroege embryo. De draaiing draait het voorste hoofd (met het gezicht en de hersenen) met de klok mee en de rest van de buitenkant van het lichaam tegen de klok in, zodat het gewervelde lichaam aan de buitenkant symmetrisch is. Omdat er geen evolutionaire druk op het hart en de inwendige organen is voor bilaterale symmetrie, worden deze lichaamsdelen uitgesloten van de draaiing en blijven ze asymmetrisch.[11]
Bij de draaiing van het hart ontstaan in het pericard de sinus transversus en de sinus obliquus. De sinus transversus is de tunnelvormige doorgang posterieur aan de aorta en de longstam, en anterieur aan de bovenste holle ader.[12][13] Deze sinus is klinisch belangrijk omdat het doorvoeren van één uiteinde van de klem door de sinus en het andere uiteinde anterieur aan de aorta/longstam volledige blokkering van de bloeduitstroom mogelijk maakt. De sinus obliquus is een omgekeerde J-vormige weerspiegeling van de holle aders en de longaders.[13] Deze ligt achter de atria (met name het linker atrium)[12] en tussen de linker en rechter longaders.
Ventrikels
[bewerken | brontekst bewerken]Sinus venosus
[bewerken | brontekst bewerken]
In het midden van de vierde week na bevruchting krijgt de sinus venosus aderlijk bloed van de polen van de rechter- en linkersinus. Elke pool ontvangt bloed van drie grote aderen: de vitelline-ader, de navelstrengader en de vena cardinal communis. (De vitelline-ader is een ader die bloed afvoert uit de dooierzak en de darmbuis tijdens de zwangerschap.) De sinusopening beweegt met de klok mee. Deze beweging wordt voornamelijk veroorzaakt door de stroming van bloed van links naar rechts, die in deaderlijke circulaie optreedt tijdens de vierde en vijfde week van de ontwikkeling.[14]
Wanneer de vena cardinal communis in de tiende week verdwijnt, blijven alleen de schuine ader van het linkeratrium en de sinus coronarius over. De rechterpool voegt zich bij het rechteratrium om het wandgedeelte van het rechteratrium te vormen. De rechter- en linker klepader fuseren en vormen een uitsteeksel dat bekendstaat als het septum spurium. In het begin zijn deze kleppen groot, maar na verloop van tijd fuseren de linker klepader en het septum spurium met het zich ontwikkelende atrium septum. De bovenste rechter klepader verdwijnt, terwijl de onderste klepader evolueert naar de onderste klep van de holle ader en de coronaire sinusklep.[14]
Hartwand
[bewerken | brontekst bewerken]De belangrijkste wanden van het hart worden gevormd tussen dag 27 en 37 na de bevruchting. De groei bestaat uit twee weefselmassa's die actief groeien en elkaar naderen totdat ze samensmelten en iets splitsen in twee afzonderlijke kanalen. Weefselmassa's die endocardiale kussens worden genoemd, ontwikkelen zich tot atrioventriculaire en conotruncale regio's. Op deze plaatsen zullen de kussens helpen bij de vorming van het auriculaire septum, ventriculaire aders, atrioventriculaire kleppen en aorta- en longaders.[15]
Atria
[bewerken | brontekst bewerken]Het boezemtussenschot ontwikkelt zich gedurende de eerste en de tweede maand (na de bevruchting) van de foetale ontwikkeling in een aantal fases. Eerst ontwikkelt zich het septum primum, een halvemaanvormig stukje weefsel, dat de eerste scheiding tussen linker en rechterboezem gaat vormen. Omdat het halvemaanvormig is, wordt de verbinding tussen de beide boezems niet geheel afgesloten; de opening die nog blijft heet ostium primum of foramen primum. Gedurende de foetale ontwikkeling kan via deze opening bloed van de rechterboezem naar de linker stromen. Terwijl het septum primum groeit, wordt het ostium primum geleidelijk aan kleiner. Voor het echter helemaal dicht is gegroeid, ontstaat een tweede opening, het ostium secundum, zodat bloed van recht naar links kan blijven stromen.[15] Rechts van het septum primum, vormt zich het septum secundum. Deze dikke, uit spierweefsel opgebouwde structuur krijgt ook een halvemaanvormige structuur, maar ontstaat aan de voorzijde, terwijl het septum primum aan de achterzijde was ontstaan. Terwijl het septum secundum groeit blijft een smalle opening open, het foramen ovale zodat het bloed van rechts naar links kan blijven stromen. Het septum secundum wordt steeds groter en de grootte van het septum primum neemt af. Uiteindelijk is van het septum primum nog slechts een klein randje over aan de linkerkant. Dit wordt de klep van het foramen ovale genoemd. Het foramen ovale opent en sluit als reactie op het drukverschil als tussen het linker- en het rechter atrium (boezem). Als de druk in het rechteratrium hoger is, gaat de klep open en als de druk daar lager is sluit de klep in reactie tot de hogere druk die na de geboorte ontstaat. Omdat de longen voor de geboorte niet functioneren, is de druk in het rechteratrium dan hoog.
Ductus Botalli
[bewerken | brontekst bewerken]Tijdens het foetale leven vindt geen oxygenatie (zuurstof in het bloed, koolstofdioxide eruit) via de longen plaats, maar via de placenta. De foetale bloedsomloop verloopt dan ook anders dan de bloedsomloop na de geboorte. De Ductus Botalli (vernoemd naar Leonardo Botallo) speelt hier een belangrijke rol bij. De ductus Botalli is een wijd bloedvat met een gespierde wand, dat een verbinding vormt tussen de stam van de longslagader en de aorta.
De longen zijn voor de geboorte nog niet volledig ontplooid, daarom is er grote weerstand in de bloedvaten van de longen. Hierdoor stroomt het bloed niet goed van het rechterventrikel via de longslagader naar de longen en dus dreigt de rechterharthelft te zwaar belast te worden. Via de ductus Botalli kan bloed van de longslagader via de aorta naar de grote bloedsomloop afvloeien, zonder de longen te passeren, zodoende wordt de rechterharthelft ontlast. Een vergelijkbare functie is de verbinding tussen beide boezems: het foramen ovale.
Ventrikels
[bewerken | brontekst bewerken]Aanvankelijk ontwikkelt zich een enkele longader in de vorm van een uitstulping in de achterwand van het linker atrium. Deze ader zal verbinding maken met de aderen van de zich ontwikkelende longknoppen. Naarmate de ontwikkeling vordert, worden de longader en zijn vertakkingen opgenomen in het linker atrium en vormen ze beide de gladde wand van het atrium. Het embryonale linker atrium blijft het trabeculaire linker atriumaanhangsel en het embryonale rechter atrium blijft het rechter atriumaanhangsel.[16]
Tussenschotvorming van het atrioventriculaire kanalen
[bewerken | brontekst bewerken]Aan het einde van de vierde week (na de bevruchting) verschijnen er twee atrioventriculaire endocardiale kussens. Aanvankelijk geeft de atrioventriculaire ader toegang tot het primitieve linkerventrikel en wordt het gescheiden van de arteriële bulbus door de rand van de ventriculaire bulbus. In de vijfde week eindigt het achterste uiteinde in het middelste deel van het bovenste endocardiale kussen. Hierdoor kan bloed zowel het linker primitieve ventrikel als het rechter primitieve ventrikel bereiken. Terwijl het voorste en achterste kussen naar binnen uitsteken, smelten ze samen om een rechter en linker atrioventriculair kanaal te vormen.[17]
Atrioventriculaire kleppen
[bewerken | brontekst bewerken]Bij de vorming van intra-atriale tussenschotten zullen atrioventriculaire kleppen beginnen te groeien. Een gespierd kamertussenschot begint te groeien van het gemeenschappelijke ventrikel naar de atrioventriculaire endocardiale kussens. De deling begint in het gemeenschappelijke ventrikel waar een groef in het buitenste oppervlak van het hart zal verschijnen, het primaire interventriculaire foramen verdwijnt uiteindelijk. (Het primaire interventriculaire foramen is een tijdelijke opening tussen de zich ontwikkelende ventrikels van het hart.) Deze sluiting wordt bereikt door verdere groei van het gespierde kamertussenschot, een bijdrage van rompkam-kegelweefsel en een membraancomponent.[18]
Kleppen en uitstroombanen
[bewerken | brontekst bewerken]Stamtussenschotvorming en arteriële kegel
[bewerken | brontekst bewerken]De arteriële kegel wordt gesloten door de conus arteriosus kussens. De stamkegels worden gesloten door de vorming van een conus arteriosusstamtussenschot, dat is gemaakt van een recht proximaal deel en een distaal spiraalvormig deel. Vervolgens bevindt het smalste deel van de aorta zich in het linker en dorsale deel. Het distale deel van de aorta wordt naar rechts naar voren geduwd. De proximale longslagader is rechts en ventraal, en het distale deel van de longslagader bevindt zich in het linker dorsale deel.[15]
Kloppen van het hart
[bewerken | brontekst bewerken]

Het menselijke embryonale hart vertoont hartactiviteit ongeveer 21 dagen na de bevruchting en bestaat dan nog alleen uit de primitieve hartbuis. Het is zichtbaar vanaf ongeveer vijf weken na de bevruchting. De ritmische elektrische depolarisatiegolven die spiercontractie activeren zijn myogeen, wat betekent dat ze spontaan in de hartspier beginnen en vervolgens verantwoordelijk zijn voor het overbrengen van signalen van cel naar cel. Spiercellen, die in de primitieve hartbuis zijn gevormd, beginnen te kloppen terwijl ze met elkaar verbonden zijn door hun wanden in een syncytium. Spiercellen initiëren ritmische elektrische activiteit, vóór de fusie van de endocardiale buizen. De hartslag begint in het gebied van de gangmaker dat een spontane depolarisatietijd heeft die sneller is dan de rest van het hartspierweefsel.[19]
Het primitieve ventrikel fungeert als initiële gangmaker. Maar deze gangmakeractiviteit wordt in feite verkregen door een groep cellen die afkomstig zijn van de sinoatriale rechter sinus venosus. Deze cellen vormen op de linker ventrikelklep een ovale sinusknoop. Na de ontwikkeling van de sinusknoop beginnen de bovenste endocardiale kussens de atrioventriculaire knoop te vormen. Met de ontwikkeling van de sinusknoop begint een band van gespecialiseerde geleidende cellen zich te vormen die de bundel van His vormen met een tak naar het rechterventrikel en een naar het linkerventrikel. De meeste geleidingswegen ontspringen aan het cardiogene mesoderm, maar de sinusknoop kan afkomstig zijn van de neurale lijst.[19]
Het menselijk hart begint te kloppen met een snelheid die dicht bij die van de moeder ligt, ongeveer 75-80 slagen per minuut (BPM). De embryonale hartslag (EHR) versnelt vervolgens lineair gedurende de eerste maand van het kloppen, met een piek van 165-185 BPM tijdens de vroege 7e week na de bevruchting. Deze versnelling is ongeveer 3,3 BPM per dag, of ongeveer 10 BPM elke drie dagen, een toename van 100 BPM in de eerste maand.[18] Na een piek van ongeveer 7,2 weken na de bevruchting, vertraagt het tot ongeveer 150 BPM (+/-25) tijdens de 13e week na de bevruchting. Na de 13e week vertraagt de vertraging en bereikt uiteindelijk een gemiddelde snelheid van ongeveer 145 (+/-25) BPM tijdens de zwangerschap.
Aangeboren hartafwijkingen
[bewerken | brontekst bewerken]In Nederland heeft ongeveer één op de honderd pasgeboren baby's een aangeboren hartafwijking. Aangeboren hartafwijkingen zijn onder andere:[20]
- Aortastenose is een vernauwing van de uitstroomopening van het linkerventrikel.
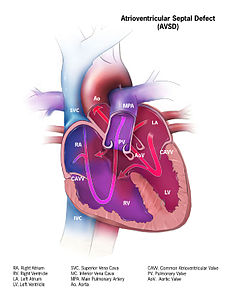
- Atrioventriculair-septumdefect (AVSD), waarbij er gaten zijn ontstaan in de tussenschotten van de atria en de ventrikels. In plaats van twee afzonderlijke kleppen is er één grote klep ontstaan, die ook nog vaak lekt.
- Atriumseptumdefect (ASD), waarbij in de scheidingswand tussen de twee atria een gaatje zit.
- Coarctatio aortae, waarbij de aorta is vernauwd doorgaans ter plaatse van de ductus van Botalli.
- Hypoplastisch linkerhartsyndroom (HLHS), waarbij de linkerhelft van het hart en de aorta niet goed ontwikkeld zijn.
- Persisterende ductus arteriosus (PDA) of open ductus Botalli, waarbij de verbinding tussen de lichaamsslagader en de longslagader na de geboorte open blijft.
- Tetralogie van Fallot
- Ventrikelseptumdefect (VSD), waarbij er een gaatje aanwezig is in het kamertussenschot van de twee ventrikels
- Pulmonalisstenose, waarbij de uitstroom uit de rechterventrikel wordt bemoeilijkt door een vernauwing bij of net onder de pulmonalisklep, de klep tussen de rechterhartkamer en de longslagader.
- De aorta bevindt zich over het septaal defect, in plaats van in de linkerventrikel (dit wordt ook wel een overrijdende aorta genoemd).
- De rechterventrikel is gespierder dan normaal (hypertrofie van de rechterventrikel).
- Transpositie van de grote vaten, waarbij de aorta en de longslagader zijn omgewisseld.
- Syndroom van Eisenmenger kenmerkt zich door secundaire, irreversibele longvaatafwijkingen als gevolg van een aangeboren hartafwijking, vaak een ventrikelseptumdefect, pulmonale hypertensie en een verloop van links-rechtsshunt, naar een bidirectionele shunt en ten slotte naar een rechts-linksshunt.
- Syndroom van Holt-Oram, vijfenzeventig procent van de getroffen personen heeft ook aangeboren afwijkingen, meestal is er geen scheiding tussen de linker- en rechterhartkamer.[21]
-
Hypoplastisch linkerhartsyndroom
-
Atrioventriculair-septumdefect
-
Coarctatio aortae
-
Transpositie van de grote vaten
Zie ook
[bewerken | brontekst bewerken]Externe link
[bewerken | brontekst bewerken]- ↑ a b c d e f g h Betts JG (2013). Anatomy & physiology, 787–846. ISBN 978-1938168130. Geraadpleegd op 11 August 2014.
- ↑ a b c Hosseini HS, Garcia KE, Taber LA (July 2017). A new hypothesis for foregut and heart tube formation based on differential growth and actomyosin contraction. Development 144 (13): 2381–2391. PMID 28526751. PMC 5536863. DOI: 10.1242/dev.145193.
- ↑ Anderson RH, Webb S, Brown NA, Lamers W, Moorman A (August 2003). Development of the heart: (2) Septation of the atriums and ventricles. Heart 89 (8): 949–958. PMID 12860885. PMC 1767797. DOI: 10.1136/heart.89.8.949.
- ↑ Schneider VA, Mercola M (February 2001). Wnt antagonism initiates cardiogenesis in Xenopus laevis. Genes & Development 15 (3): 304–315. PMID 11159911. PMC 312618. DOI: 10.1101/gad.855601.
- ↑ Marvin MJ, Di Rocco G, Gardiner A, Bush SM, Lassar AB (February 2001). Inhibition of Wnt activity induces heart formation from posterior mesoderm. Genes & Development 15 (3): 316–327. PMID 11159912. PMC 312622. DOI: 10.1101/gad.855501.
- ↑ Animal Tissues. Users.rcn.com (13 augustus 2010). Gearchiveerd op 5 mei 2009. Geraadpleegd op 17 oktober 2010.
- ↑ a b c Sadler TW (2012). Langman. Embriología Médica. Lippincott Williams & Wilkins, p. 165. ISBN 978-84-96921-46-7.
- ↑ Larsen W (2001). Human Embryology, 3rd. Elsevier Saunders, 159–163. ISBN 978-0-443-06583-5.
- ↑ Main Frame Heart Development. Meddean.luc.edu. Geraadpleegd op 17 oktober 2010.
- ↑ Rohen J, Lutjen E (2008). Embriología functional: una perspectiva desde la biología del desarrollo. Panamericana, p. 70. ISBN 978-84-9835-155-2.
- ↑ de Lussanet MH, Osse JW (2012). An ancestral axial twist explains the contralateral forebrain and the optic chiasm in vertebrates. Animal Biology 62 (2): 193–216. DOI: 10.1163/157075611X617102.
- ↑ a b Issa, Ziad F.; Miller, John M.; Zipes, Douglas P. (2019-01-01), Issa, Ziad F.; Miller, John M.; Zipes, Douglas P., reds., "27 - Epicardial Ventricular Tachycardia", Clinical Arrhythmology and Electrophysiology (Third Edition) (in Engels), Philadelphia: Elsevier, pp. 907–924, doi:10.1016/b978-0-323-52356-1.00027-x, ISBN 978-0-323-52356-1, bezocht 2020-11-16
- ↑ a b Klick, John C.; Ali, Jafer; Avery, Edwin G. (2014-01-01), Reich, David L.; Fischer, Gregory W., reds., "23 - Echocardiographic Evaluation of Pericardial Disease", Perioperative Transesophageal Echocardiography (in Engels), Philadelphia: W.B. Saunders, pp. 253–264, doi:10.1016/b978-1-4557-0761-4.00023-2, ISBN 978-1-4557-0761-4, bezocht 2020-11-16
- ↑ a b Carlson B (2012). Embriología humana y biología del desarrollo. Mosby, p. 451. ISBN 978-84-8174-785-0.
- ↑ a b c Fernández PM (2002). Manual de biología del desarrollo. Manual Moderno, p. 243. ISBN 978-968-426-976-7.
- ↑ Eynard A, Valentich M, Rovasio R (2011). Histología y embriología del ser humano: bases celulares y moleculares. Panamericana, p. 283. ISBN 978-950-06-0602-8.
- ↑ Moore KL, Persaud TV (2008). Embriología Clínica. Elsevier Saunders, p. 245. ISBN 978-84-8086-337-7.
- ↑ Tellez de Peralta G (2003). Tratado de cirugía cardiovascular. Díaz de Santos, p. 44.
- ↑ a b Larsen W (2003). Embriología humana. Elsevier Science, p. 177. ISBN 978-968-426-976-7.
- ↑ Aangeboren hartafwijkingen
- ↑ syndroom van Holt-Oram Otphanet