Homologace
Homologace nebo homologační reakce je každá chemická reakce, při které se reaktant mění na následující člen homologické řady, tedy skupiny sloučenin lišících se o stejnou skupinu atomů, což je často skupina -CH2-; k homologaci dochází, když se přidávají další takové jednotky. Nejčastěji se provádějí homologace navyšující počet methylenových (-CH2-) skupin v nasyceném řetězci.[1] Jako příklad lze uvést reakce aldehydů a ketonů s diazomethanem či methoxymethylentrifenylfosfinem.
Příklady
[editovat | editovat zdroj]- Kilianiova-Fischerova syntéza, kde se molekula aldózy prodlužuje v trojfázovém procesu skládajícím se z:
- nukleofilní adice kyanidu na karbonyl za vzniku kyanohydrinu
- hydrolýzy na lakton
- redukce na homologní aldózu
- Wittigova reakce aldehydu s methoxymethylentrifenylfosfinem, jejím produktem je homologní aldehyd.
- Arndtova–Eistertova reakce je posloupnost chemických reakcí sloužících k přeměně karboxylových kyselin na vyšší homology (obsahující o jeden atom uhlíku více)
- Kowalského homologace esterů, alternativa Arndtovy-Eistertovy syntézy. Používá se na přípravu β-aminoesterů z α-aminoesterů a probíhá přes ynolátový meziprodukt.[2]
- Seyferthova–Gilbertova homologace, přeměna aldehydu na koncový alkyn, jenž se následně mění na homologní aldehyd.
Některé reakce prodlužují řetězec o více než jednu jednotku.
Zkracování řetězce
[editovat | editovat zdroj]Délkku řetězce lze také zkracovat:
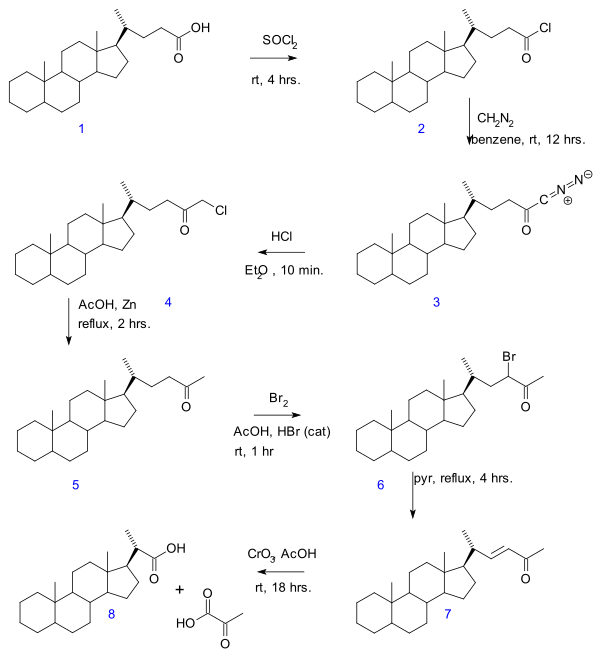
- V Gallagherově–Hollanderově degradaci se odštěpuje kyselina pyrohroznová z lineární alifatické karboxylové kyseliny za vzniku nové kyseliny obsahující o dva atomy uhlíku méně.[3] V původní práci byla popsána přeměna žlučové kyseliny v posloupnosti reakcí začínající tvorbou acylchloridu (2) působením chloridu thionylu, po níž následuje vznik diazoketonu (3) reakcí s diazomethanem, jeho přeměna na chlormethylketon (4) reakcí s kyselinou chlorovodíkovou, redukce na methylketon (5), halogenace ketonu na 6, eliminační reakce s pyridinem za tvorby enonu 7 a konečná oxidace oxidem chromovým na kyselinu bisnorcholanovou 8.
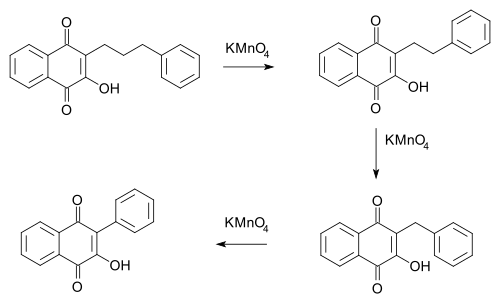
Při Hookerově reakci je alkyllový řetězec derivátu naftochinonu (poprvé to bylo pozorováno u lapacholu) ochuzen o jednu methylenovou jednotku, která je manganistanem draselným oxidována na oxid uhličitý.[4][5]
- Z mechanistického hlediska oxidace způsobuje štěpení kruhu na alkenové skupině, po němž následuje dekarboxylace (odštěpení oxidu uhličitého) a uzavření kruhu.
Odkazy
[editovat | editovat zdroj]Související články
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Homologation reaction na anglické Wikipedii.
- ↑ Encyclopedia of Inorganic Chemistry DOI:10.1002/0470862106.id396
- ↑ D. Gray; C. Concellon; T. Gallagher. Kowalski Ester Homologation. Application to the Synthesis of β-Amino Esters. The Journal of Organic Chemistry. 2004, s. 4849–4851. DOI 10.1021/jo049562h. PMID 15230615.
- ↑ Vincent P. Hollander and T. F. Gallagher PARTIAL SYNTHESIS OF COMPOUNDS RELATED TO ADRENAL CORTICAL HORMONES. VII. DEGRADATION OF THE SIDE CHAIN OF CHOLANIC ACID Journal of Biological Chemistry, Mar 1946; 162: 549 - 554 Link Archivováno 7. 1. 2009 na Wayback Machine.
- ↑ On the Oxidation of 2-Hydroxy-1,4-naphthoquinone Derivatives with Alkaline Potassium Permanganate Samuel C. Hooker Journal of the American Chemical Society 1936; 58(7); 1174-1179. DOI:10.1021/ja01298a030
- ↑ On the Oxidation of 2-Hydroxy-1,4-naphthoquinone Derivatives with Alkaline Potassium Permanganate. Part II. Compounds with Unsaturated Side Chains Samuel C. Hooker and Al Steyermark Journal of the American Chemical Society 1936; 58(7); pp 1179 - 1181; DOI:10.1021/ja01298a031