Ammoniumhydrogendifluorid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
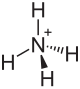 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Ammoniumhydrogendifluorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | NH4HF2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 57,04 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,5 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
230 °C (Zersetzung)[1] | ||||||||||||||||||
| Löslichkeit |
gut in Wasser (630 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
1 mg·m−3[1] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Ammoniumhydrogendifluorid ist ein saures Ammoniumsalz der Fluorwasserstoffsäure.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ammoniumhydrogendifluorid bildet farblose, leicht zerfließende, in Wasser leicht lösliche Kristalle. Es ätzt Glas und wird des Weiteren industriell zur Fleckenentfernung und in der Erdölindustrie verwendet, um sich durch Granitschichten zu arbeiten. Die das Siliciumdioxid angreifende Spezies ist das HF2--Anion.[3] Es ist der aktive Bestandteil verschiedener Ätzmischungen zum selektiven Ätzen von Silciumdioxidschichten in der Halbleiterindustrie.[4]
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Beim starken Erhitzen zerfällt es in Ammoniak und Fluorwasserstoff.[1]
Synthese
[Bearbeiten | Quelltext bearbeiten]Die Darstellung von Ammoniumhydrogendifluorid erfolgt durch Umsetzung von wässriger Ammoniaklösung mit Flusssäure im Molverhältnis 1 : 2 und anschließender Kristallisation aus Wasser.[5]
Vorsichtsmaßnahmen
[Bearbeiten | Quelltext bearbeiten]Ammoniumhydrogendifluorid ist ätzend und giftig. Berühren mit Haut und Augen vermeiden. Nicht verschlucken.[1]
Entsorgung
[Bearbeiten | Quelltext bearbeiten]Gelöstes Fluorid wird als Calciumfluorid ausgefällt.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]- Dreizentrenbindung, zum Hydrogendifluorid-Anion
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k Eintrag zu Ammoniumhydrogendifluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu Ammonium hydrogendifluoride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ The Electrochemical Society: Cleaning Technology in Semiconductor Device Manufacturing. The Electrochemical Society, 2000, ISBN 978-1-566-77259-4, S. 248 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Tadahiro Ohmi: Scientific Wet Process Technology for Innovative LSI/FPD Manufacturing. CRC Press, 2016, ISBN 978-1-420-02686-3, S. 178 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Alain Tressaud: Functionalized Inorganic Fluorides Synthesis, Characterization and Properties of Nanostructured Solids. John Wiley & Sons, 2010, ISBN 0-470-66075-9, S. 210 (eingeschränkte Vorschau in der Google-Buchsuche).

