Kaempferol
| Kaempferol | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 3,5,7-trihidroxi-2-(4-hidroxifenyl)-4H-1-benzopiran-4-ona | ||
| General | ||
| Fórmula semidesarrollada | C15H10O6 | |
| Fórmula estructural |
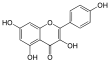 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 520-18-3[1] | |
| ChEBI | 28499 | |
| ChEMBL | CHEMBL150 | |
| ChemSpider | 4444395 | |
| DrugBank | DB01852 | |
| PubChem | 5280863 | |
| UNII | 731P2LE49E | |
| KEGG | C05903 | |
| Propiedades físicas | ||
| Apariencia | Sólido cristalino amarillo. | |
| Masa molar | 286,23 g/mol | |
| Punto de fusión | 549 K (276 °C) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El kaempferol es un flavonol, que ha sido aislado de diversas fuentes: Té verde,[2] Delphinium,[3] brócoli, avellana de brujas (Hamamelis virginiana), toronja,[4] uva, coles de Bruselas, manzanas y otras tantas fuentes. Es altamente soluble en agua y es soluble en etanol caliente y éter etílico. Muchos glucósidos del kaempferol, tales como la kaempferitrina y la astragalina, han sido aislados de productos naturales de plantas.
El Kaempferol es el compuesto que confiere su color a las flores de Acacia decurrens y Acacia longifolia[5] El compuesto tiene propiedades antidepresivas.[6]
Un estudio reveló que tres flavonoles (kaempferol, quercetina, y miricetina) reducen el riesgo de cáncer pancreático en un 23%.[7]
Investigadores de la Universidad de California en Los Ángeles encontraron que los participantes del estudio, los cuales ingerían frutas con cierto contenido de flavonoides, mostraban protección al desarrollo del cáncer de pulmón. El Dr. Zuo-Feng Zhang, del Centro Jonsson del Cáncer, en la Universidad de California en Los Ángeles argumentó que los flavonoides con mayor efecto protector fueron la catequina (Presente en fresas y tés negro y verde), el kaempferol, encontrado en uvas, coles de Bruselas y manzanas, y la quercetina, presente en alubias, cebollas y manzanas.[8][9]
Biosíntesis
[editar]
Debido a que el kaempferol es un flavonol, tiene su origen a partir un policétido que contiene ácido 4-hidroxicinámico como iniciador. Este compuesto evoluciona a la chalcona de la naringenina por acción de la naringenina-chalcona sintasa (EC 2.3.1.74). Posteriormente la chalcona sufre isomerización a naringenina con la catálisis de la chalcona isomerasa (EC 5.5.1.6). La naringenina se hidroxila por medio de oxígeno atmosférico y la flavanona 3-hidroxilasa (EC.1.14.11.9) para dar dihidrokaempferol. La flavonol sintasa (EC 1.14.11.23) concluye la ruta, deshidrogenando al precursor con oxígeno atmosférico.[10]
Producción natural
[editar]Kaempferol ha sido identificado en muchas especies de plantas comúnmente utilizadas en la medicina tradicional. Ha sido encontrado en Acacia nilotica, Adansonia digitata, Albizia lebbeck, Aloe vera, Amburana cearensis, Ammi majus, Angelica keiskei, Ardisia japonica, Bauhinia forficata, Bauhinia microstachya, Capparis spinosa, Cassia alata, Centella asiatica, Chromolaena odorata, Cissus sicyoides, Coccinia grandis, Crassocephalum crepidioides, Crocus sativus, Cynanchum acutum, Cynanchum chinense, Dicliptera chinensis, Elwendia persica, Equisetum arvense, Euphorbia pekinensis, Ficaria verna, Foeniculum vulgare, Fragaria × ananassa, Fragaria vesca, Galega officinalis, Ginkgo biloba, Glycine max, Grindelia robusta, Gymnema sylvestre, Helleborus niger, Hippophae rhamnoides, Houttuynia cordata, Hypericum perforatum, Impatiens balsamina, Lamium album, Laurus nobilis, Lonicera japonica, Lycium barbarum, Lycium chinense, Lysimachia vulgaris, Malva parviflora, Peumus boldus, Phyllanthus emblica, Ribes nigrum, Salvia rosmarinus, Sambucus nigra, Sanguisorba minor, Siraitia grosvenori, Solanum nigrum, Solenostemma argel, Solidago virgaaurea, Sutherlandia frutescens, Symphytum officinale, Syzygium aromaticum, Tilia americana, Toona sinensis, Trigonella foenum-graecum, Tropaeolum majus, Tussilago farfara, Vaccinium vitis-idaea, Warburgia ugandensis y Wedelia trilobata.[11]
Referencias
[editar]- ↑ Número CAS
- ↑ Jun Seong Park, Ho Sik Rho, Duck Hee Kim, and Ih Seop Chang (2006). «Enzymatic Preparation of Kaempferol from Green Tea Seed and Its Antioxidant Activity». J. Agric. Food Chem. 54 (8): 2951-2956. PMID 16608214. doi:10.1021/jf052900a.
- ↑ A. G. Perkin, E. J. Wilkinson (1902). J. Chem. Soc. 81: 585.
- ↑ Dunlap, Wender (1962). Anal. Biochem. 4: 110.
- ↑ Lycaeum -- Phytochemistry Intro Archivado el 30 de septiembre de 2007 en Wayback Machine.
- ↑ «ANTIDEPRESSANT EFFECT OF KAEMPFEROL, A CONSTITUENT OF SAFFRON (CROCUS SATIVUS) PETAL, IN MICE AND RATS». Pharmacologyonline.
- ↑ Ute Nöthlings, Suzanne P. Murphy, Lynne R. Wilkens, Brian E. Henderson & Laurence N. Kolone. 2007. Flavonols and Pancreatic Cancer Risk. American Journal of Epidemiology 166(8): 924–931. doi 10.1093/aje/kwm172
- ↑ «UCLA news - Fruits, vegetables, teas may protect smokers from lung cancer». Archivado desde el original el 13 de febrero de 2012. Consultado el 31 de diciembre de 2010.
- ↑ [Kaempferol treatment increased the expression and the mitochondria localization of the NAD-dependent deacetylase SIRT3. The chronic myelogenous leukemiae K562 cells stably overexpressing SIRT3 were more sensitive to kaempferol, whereas SIRT3 silencing did not increase the resistance of K562 cells to kaempferol ( Marfe G et al. 2009).]
- ↑ Paul M. Dewick (2009). Medicinal Natural Products: A Biosynthetic Approach, Third Edition. New Jersey, EU: John Wiley and Sons. ISBN 978-0-470-74167-2.
- ↑ Calderon-Montaño JM, Burgos-Moron E, Perez-Guerrero C, Lopez-Lazaro M. (2011). "A review on the dietary flavonoid kaempferol.". Mini Rev Med Chem. 11 (4): 298–344. doi:10.2174/138955711795305335. PMID 21428901.