نفتالین
| نفتالین | |||
|---|---|---|---|
| |||
| |||
| |||
Naphthalene[۱] | |||
Bicyclo[4.4.0]deca-13579-pentaene | |||
دیگر نامها white tar camphor tar tar camphor naphthalin naphthaline antimite albocarbon hexalene mothballs moth flakes | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۹۱-۲۰-۳ | ||
| پابکم | ۹۳۱ | ||
| کماسپایدر | ۹۰۶ | ||
| UNII | 2166IN72UN | ||
| شمارهٔ ئیسی | 214-552-7 | ||
| KEGG | C00829 | ||
| ChEBI | CHEBI:16482 | ||
| ChEMBL | CHEMBL۱۶۲۹۳ | ||
| شمارهٔ آرتیئیسیاس | QJ0525000 | ||
| 1421310 | |||
| 3347 | |||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | C10H۸ | ||
| جرم مولی | ۱۲۸٫۱۷ g mol−1 | ||
| شکل ظاهری | بلور یا پرک های سفید رنگ | ||
| بوی | بوی قوی قطران ذغال سنگ | ||
| چگالی | 1.145 g/cm3 (15.5 °C)[۲] 1.0253 g/cm3 (20 °C)[۳] 0.9625 g/cm3 (100 °C)[۲] | ||
| دمای ذوب | ۷۸٫۲ درجه سلسیوس (۱۷۲٫۸ درجه فارنهایت؛ ۳۵۱٫۳ کلوین) ۸۰٫۲۶ درجه سلسیوس (۱۷۶٫۴۷ درجه فارنهایت؛ ۳۵۳٫۴۱ کلوین) at 760 mmHg[۳] | ||
| دمای جوش | ۲۱۷٫۹۷ درجه سلسیوس (۴۲۴٫۳۵ درجه فارنهایت؛ ۴۹۱٫۱۲ کلوین) at 760 mmHg[۲][۳] | ||
| انحلالپذیری در آب | 19 mg/L (10 °C) 31.6 mg/L (25 °C) 43.9 mg/L (34.5 °C) 80.9 mg/L (50 °C)[۳] 238.1 mg/L (73.4 °C)[۴] | ||
| انحلالپذیری | محلول در الکل مایع، آمونیاک، کربوکسیلیک اسیدها، بنزن، گوگرد دیاکسید، [۴] کربن تتراکلرید، کربن دیسولفید، تولوئن، آنیلین[۵] | ||
| انحلالپذیری در ethanol | 5 g/100 g (0 °C) 11.3 g/100 g (25 °C) 19.5 g/100 g (40 °C) 179 g/100 g (70 °C)[۵] | ||
| انحلالپذیری در acetic acid | 6.8 g/100 g (6.75 °C) 13.1 g/100 g (21.5 °C) 31.1 g/100 g (42.5 °C) 111 g/100 g (60 °C)[۵] | ||
| انحلالپذیری در chloroform | 19.5 g/100 g (0 °C) 35.5 g/100 g (25 °C) 49.5 g/100 g (40 °C) 87.2 g/100 g (70 °C)[۵] | ||
| انحلالپذیری در hexane | 5.5 g/100 g (0 °C) 17.5 g/100 g (25 °C) 30.8 g/100 g (40 °C) 78.8 g/100 g (70 °C)[۵] | ||
| انحلالپذیری در butyric acid | 13.6 g/100 g (6.75 °C) 22.1 g/100 g (21.5 °C) 131.6 g/100 g (60 °C)[۵] | ||
| log P | 3.34[۳] | ||
| فشار بخار | 8.64 Pa (20 °C) 23.6 Pa (30 °C) 0.93 kPa (80 °C)[۴] 2.5 kPa (100 °C)[۶] | ||
| kH | 0.42438 L·atm/mol[۳] | ||
| پذیرفتاری مغناطیسی | -91.9·10-6 cm3/mol | ||
| رسانندگی گرمایی | 98 kPa: 0.1219 W/m·K (372.22 K) 0.1174 W/m·K (400.22 K) 0.1152 W/m·K (418.37 K) 0.1052 W/m·K (479.72 K)[۷] | ||
| ضریب شکست (nD) | 1.5898[۳] | ||
| گرانروی | 0.964 cP (80 °C) 0.761 cP (100 °C) 0.217 cP (150 °C)[۸] | ||
| ساختار | |||
| ساختار بلوری | دستگاه بلوری تکشیب[۹] | ||
| گروه فضایی | P21/b[۹] | ||
| Point group | C52h[۹] | ||
| ثابت شبکه | a = 8.235 Å, b = 6.003 Å, c = 8.658 Å[۹] | ||
| Lattice constant | α = 90°, β = 122.92°, γ = 90° | ||
| ترموشیمی | |||
| 165.72 J/mol·K[۳] | |||
آنتروپی مولار
استاندارد S |
167.39 J/mol·K[۳][۶] | ||
آنتالپی استاندارد
تشکیل ΔfH |
78.53 kJ/mol[۳] | ||
انرژی آزاد گیبس (ΔG)
|
201.585 kJ/mol[۳] | ||
| Std enthalpy of combustion ΔcH |
-5156.3 kJ/mol[۳] | ||
| خطرات | |||
| GHS pictograms |     [۱۰] [۱۰]
| ||
| سیستم هماهنگ جهانی طبقهبندی و برچسبگذاری مواد شیمیایی | Danger | ||
| GHS hazard statements | H228, H302, H351, H410[۱۰] | ||
| GHS precautionary statements | P210, P273, P281, P501[۱۰] | ||
| خطرات اصلی | Flammable, sensitizer, possible ماده سرطانزا. Dust can form مواد منفجره mixtures with جو زمین | ||
| لوزی آتش | |||
| نقطه اشتعال | |||
| دمای خودآتشگیری | |||
| محدودیتهای انفجار | 5.9%[۱۰] | ||
| آمریکا Permissible exposure limit (PEL) |
TWA 10 ppm (50 mg/m3)[۱۱] | ||
| Threshold Limit Value | 10 ppm[۳] (TWA), 15 ppm[۳] (STEL) | ||
| LD50 | 1800 mg/kg (rat, oral) 490 mg/kg (rat, oral) 1200 mg/kg (guinea pig, oral) 533 mg/kg (mouse, oral)[۱۲] | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
نفتالین یا نفتالن (نام ترجیحی آیوپاک) که به نامهای «آلبوکربن»، «کافور قیر» یا «قیر سفید» نیز شناخته میشود؛ یک هیدروکربن آروماتیک است که به شکل گلولههای کوچک به بازار میآیند و حالت جامد و رنگ سفیدی دارد. نفتالین به تندی تصعید میشود و بخاری بسیار آتش زا دارد. مولکول نفتالین از دو حلقهٔ جوش خوردهٔ بنزن ساخته شدهاست. از زغالسنگ به دست میآید و به فتالیک انیدرید برای ساخت پلاستیکها، رنگها و حلکنندهها به کار میرود. نفتالین برای گندزدایی و حشره کشی (بیشتر حل شده در متانول) کاربرد فراوانی دارد. نفتالین را برای جلوگیری از بید زدن فرش و پارچههای پشمی نیز به کار میبرند. نفتالین خاصیت حشره کش بسیار ضعیفی دارد، گرچه در قدیم برای این منظور زیاد استفاده میشده است. [۱۳]
تاریخچه
[ویرایش]سال ۱۸۱۹ و ۱۸۲۰، دست کم دو شیمیدان مادهٔ جامد سفیدی با بوی زننده گزارش کردند که از تقطیر زغال سنگ به دست میآید. سال ۱۸۲۱، جان کید(John Kidd) بسیاری از ویژگیهای این مادهها و روشهای فرآوری آنها پیدا کرد و نام نفتالین را برای این ماده پیشنهاد کرد (چون این ماده از گونهای نفتا -که نام گستردهای که برای آمیختهای از هیدروکربنهای فرار و آتشگیر که زغال سنگ را نیز دربرمی گیرند؛ میشود. - به دست آمده بود) در ادامه فرمول شیمیایی آن توسط مایکل فارادی (Michael Faraday) در سال ۱۸۲۶ کشف شد. ساختار مولکولل آن نیز در سال ۱۸۶۶ توسط امیل ارلنمایر (Emil Erlenmeyer) کشف و سه سال بعد توسط کارل گریب (Carl Gräbe) تأیید شد. همچنین این ماده بهطور اتفاقی از روی میز داروخانه چی بر روی زمین افتاد و فردا صبح وی با جسد کشته شدهٔ چند سوسک مواجه شد. از آن پس در گند زدایی و دفع حشرات نیز مورد استفاده قرار میگیرد.
هشدار
[ویرایش]طبق نظر «آژانس مواد شیمیایی اروپا»، نفتالین ماده ایست بسیار سمی. نفتالین به پوست انسان صدمه سنگینی میزند. ایست تنفسی، صدمههای جبرانناپذیر به کبد، کلیه، چشم و روده از دیگر عوارض خطرناک نفتالین هستند.[۱۴] این ماده شیمیایی سمی هیچ گونه جایگاه معتبری برای مصرف خانگی ندارد و نبایستی در خانه نگهداری یا مصرف شود. نفتالین به دلیل دارا بودن مواد نفتی باعث خورندگی میشود و عمر مفید اورینگ ها و کاسه نمد ها را در صنعت کاهش می دهد .
منابع تولید
[ویرایش]گذشته از قطران زغال سنگ، مقدار بسیار کم از نفتالین توسط magnolias و انواع خاصی از آهو و هم چنین توسط موریانه قنات در برابر مورچهها و قارچهای سمی تولید میشود. نفتالین در شهاب سنگها نیز یافت میشود.[۱۵]
ساختار شیمیایی
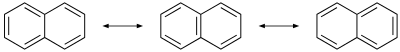
[ویرایش]نفتالن (نفتالین) مادهای مولکولی با فرمول C10H8 است که در گروه مواد آلی آروماتیک قرار میگیرد. مولکولهای این ماده از دو حلقهٔ بنزنی ساخته شدهاند که در یک پیوند C-C مشترک هستند (به هم جوش خوردهاند). بنابراین این مولکول هم مانند بنزن دارای «رزونانس» است.[۱۶] سه ساختار رزونانسی این مولکول به شکل زیر هستند:
به خاطر وجود این ساختارها، نفتالن دارای دو طول مختلف برای پیوندهای C-C است.[۱۷]
واکنشهای شیمیایی
[ویرایش]نفتالن در واکنشهای کلی و عمومی ترکیبهای آروماتیک شرکت میکند. این واکنشها از نوع جانشینی الکتروندوستی هستند که طی آن یک گونهٔ کمالکترون (الکتروندوست)، جانشین یکی از هیدروژنها در مولکول نفتالن میشود و دو نوع محصول ایزومری تولید میکند.[۱۸]
دیگر واکنشی که نفتالن در آن شرکت میکند، واکنش سوختن است که مشترک بین تقریباً تمام مواد آلی است. نفتالن مانند بیشتر مواد آروماتیک، هنگام سوختن، علاوه بر آب و دیاکسید کربن، دوده هم تولید میکند (سوختن ناقص).
منابع
[ویرایش]- ↑ Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The انجمن سلطنتی شیمی. 2014. pp. 13, 35, 204, 207, 221–222, 302, 457, 461, 469, 601, 650. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ ۲٫۰ ۲٫۱ ۲٫۲ "Ambient Water Quality Criteria for Naphthalene" (PDF). United States Environmental Protection Agency. 2014-04-23. Retrieved 2014-06-21.
- ↑ ۳٫۰۰ ۳٫۰۱ ۳٫۰۲ ۳٫۰۳ ۳٫۰۴ ۳٫۰۵ ۳٫۰۶ ۳٫۰۷ ۳٫۰۸ ۳٫۰۹ ۳٫۱۰ ۳٫۱۱ ۳٫۱۲ ۳٫۱۳ Lide, David R., ed. (2009). هندبوک شیمی و فیزیک سیآرسی (90th ed.). بوکا راتون، فلوریدا: انتشارات سیآرسی. ISBN 978-1-4200-9084-0.
- ↑ ۴٫۰ ۴٫۱ ۴٫۲ Anatolievich, Kiper Ruslan. "naphthalene". chemister.ru. Retrieved 2014-06-21.
- ↑ ۵٫۰ ۵٫۱ ۵٫۲ ۵٫۳ ۵٫۴ ۵٫۵ Seidell, Atherton; Linke, William F. (1919). Solubility of Inorganic and Organic Compounds (2nd ed.). New York: D. Van Nostrand Company. pp. 443–446.
- ↑ ۶٫۰ ۶٫۱ Naphthalene in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-24)
- ↑ "Thermal Conductivity of Naphthalene". DDBST GmbH. DDBST GmbH. Archived from the original on 4 March 2016. Retrieved 2014-06-21.
- ↑ "Dynamic Viscosity of Naphthalene". DDBST GmbH. DDBST GmbH. Archived from the original on 4 March 2016. Retrieved 2014-06-21.
- ↑ ۹٫۰ ۹٫۱ ۹٫۲ ۹٫۳ Douglas, Bodie E.; Ho, Shih-Ming (2007). Structure and Chemistry of Crystalline Solids. New York: Springer Science+Business Media, Inc. p. 288. ISBN 978-0-387-26147-8.
- ↑ ۱۰٫۰ ۱۰٫۱ ۱۰٫۲ ۱۰٫۳ کاتالوگ آنلاین زیگما بدون تاریخ.
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامPGCHوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ "Naphthalene". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Gerfried Deschka: (ضد عفونی حشرات) Die Desinfektion kleiner Insektensammlungen nach neueren Gesichtspunkten. ناشر: Steyrer Entomologenrunde. Nr. 21, Steyr 1987, صص. 57–61
- ↑ «نسخه آرشیو شده». بایگانیشده از اصلی در ۲۶ دسامبر ۲۰۱۵. دریافتشده در ۸ ژانویه ۲۰۱۶.
- ↑ متن پیوند، متن اضافی.
- ↑ General Chemistry, Chapter 28; Charles E. Mortimer
- ↑ Organic Chemistry, Chapter 14; Morrison & Boyd; 6th Edition
- ↑ Organic Chemistry, Chapter 15; Morrison & Boyd; 6th Edition
- مشارکتکنندگان ویکیپدیا. «Naphthalene». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۳ می ۲۰۱۱.