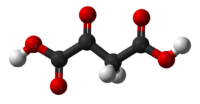
Asid oksaloasetik

| |
| |
| Nama | |
|---|---|
| Nama IUPAC pilihan
Asid 2-oksobutanadioik | |
| Nama lain
Asid oksaloasetik
Asid oksalaasetik Asid 2-oksosuksinik Asid ketosuksinik | |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.005.755 |
| Nombor EC |
|
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C4H4O5 | |
| Jisim molar | 132.07 g/mol |
| Ketumpatan | 1.6 g/cm3 |
| Takat lebur | 161 °C (322 °F; 434 K) |
| Termokimia | |
Entalpi pembentukan
piawai (ΔfH⦵298) |
-943.21 kJ/mol |
Entalpi pembakaran
piawai (ΔcH⦵298) |
-1205.58 kJ/mol |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Asid oksaloasetik (juga dikenali sebagai asid oksalasetik atau OAA) ialah sebatian organik kristal dengan formula kimia HO2CC(O)CH2CO2H. Asid oksaloasetik, dalam bentuk bes konjugatnya oksaloasetat, ialah perantara metabolisme dalam banyak proses dalam haiwan. Ia mengambil bahagian dalam glukoneogenesis, kitaran urea, kitaran glioksilat, sintesis asid amino, sintesis asid lemak dan kitaran asid sitrik.
Ciri
[sunting | sunting sumber]Asid oksaloasetik mengalami penyahprotonan berturut-turut untuk memberikan dwianion:
- HO2CC(O)CH2CO2H ⇌−O2CC(O)CH2CO2H + H+, pKa = 2.22
- −O2CC(O)CH2CO2H ⇌−O2CC(O)CH2CO2− + H+, pKa = 3.89
Dalam pH yang tinggi, proton berenol terion:
- −O2CC(O)CH2CO2−
 −O2CC(O−)CHCO2− + H+, pKa = 13.03
−O2CC(O−)CHCO2− + H+, pKa = 13.03
Bentuk enol asid oksaloasetik adalah sangat stabil. Pentautomeran keto-enol dimangkinkan oleh enzim oksaloasetat tautomerase. trans-Enol-oksaloasetat juga muncul apabila tartrat menjadi substrat kepada fumarase.[1]

Biosintesis
[sunting | sunting sumber]Oksaloasetat terbentuk dalam beberapa cara dalam alam semula jadi. Laluan utama adalah ketika pengoksidaan L-malat yang dimangkinkan oleh malat dehidrogenase dalam kitaran asid sitrik. Malat juga dioksidakan oleh suksinat dehidrogenase dalam tindak balas yang perlahan dengan produk awal ialah enol-oksaloasetat.[2] Ia juga timbul daripada pemeluwapan piruvat dengan asid karbonik, didorong oleh hidrolisis ATP:
- CH3C(O)CO2− + HCO3− + ATP → −O2CCH2C(O)CO2− + ADP + Pi
Dalam mesofil tumbuhan, proses ini diteruskan melalui fosfoenolpiruvat, dimangkinkan oleh fosfoenolpiruvat karboksilase. Oksaloasetat juga boleh timbul daripada trans- atau nyahaminasi asid aspartik.
Fungsi biokimia
[sunting | sunting sumber]Oksaloasetat ialah perantaraan kitaran asid sitrik, di mana ia bertindak balas dengan asetil-KoA untuk membentuk sitrat, dimangkinkan oleh sintase sitrat. Ia juga terlibat dalam glukoneogenesis, kitaran urea, kitaran glioksilat, sintesis asid amino dan sintesis asid lemak. Oksaloasetat juga merupakan perencat kuat kompleks II.
Glukoneogenesis
[sunting | sunting sumber]Glukoneogenesis ialah laluan metabolik yang terdiri daripada satu siri 11 tindak balas yang dimangkinkan enzim, menghasilkan penjanaan glukosa daripada substrat bukan karbohidrat. Permulaan proses ini berlaku dalam matriks mitokondrion, di mana molekul piruvat ditemui. Molekul piruvat dikarboksilasi oleh enzim piruvat karboksilase, diaktifkan oleh molekul setiap ATP dan air. Tindak balas ini mengakibatkan pembentukan oksaloasetat. NADH mengurangkan oksaloasetat kepada malat. Transformasi ini diperlukan untuk mengangkut molekul keluar dari mitokondrion. Sekali dalam sitosol, malat dioksidakan kepada oksaloasetat semula menggunakan NAD+. Kemudian, oksaloasetat kekal dalam sitosol, di mana tindak balas yang lain akan berlaku. Oksaloasetat kemudiannya dinyahkarboksil dan difosforilkan fosfoenolpiruvat karboksikinase dan menjadi 2-fosfoenolpiruvat dengan guanosina trifosfat (GTP) sebagai sumber fosfat. Glukosa diperoleh selepas pemprosesan hiliran selanjutnya.
Kitaran urea
[sunting | sunting sumber]Kitaran urea ialah laluan metabolik yang menghasilkan pembentukan urea menggunakan satu molekul ammonium daripada asid amino terdegradasi, satu lagi kumpulan ammonium daripada aspartat dan satu molekul bikarbonat. Laluan ini biasanya berlaku dalam hepatosit. Tindak balas yang berkaitan dengan kitaran urea menghasilkan NADH, dan NADH boleh dihasilkan dalam dua cara yang berbeza. Salah satu daripada ini menggunakan oksaloasetat. Dalam sitosol, terdapat molekul fumarat. Fumarat boleh diubah menjadi malat oleh tindakan enzim fumarase. Malat diproses oleh malat dehidrogenase untuk menjadi oksaloasetat, menghasilkan molekul NADH. Selepas itu, oksaloasetat akan dikitar semula menjadi aspartat kerana transaminase lebih suka asid keto ini berbanding yang lain. Kitar semula ini mengekalkan aliran nitrogen ke dalam sel.

Kitaran glioksilat
[sunting | sunting sumber]Kitaran glioksilat ialah satu varian kitaran asid sitrik.[3] Ia merupakan laluan anabolik yang berlaku dalam tumbuhan dan bakteria yang menggunakan enzim isositrat liase dan malat sintase. Beberapa langkah perantaraan kitaran berbeza sedikit daripada kitaran asid sitrik; namun oksaloasetat mempunyai fungsi yang sama dalam kedua-dua proses. Ini bermakna bahawa oksaloasetat dalam kitaran ini juga bertindak sebagai bahan tindak balas utama dan produk akhir. Sebenarnya, oksaloasetat ialah hasil bersih kitaran glioksilat kerana gelung kitarannya menggabungkan dua molekul asetil-KoA.
Sintesis asid lemak
[sunting | sunting sumber]Pada peringkat sebelumnya, asetil-KoA dipindahkan dari mitokondria ke sitoplasma, di mana adanya sintase asid lemak. Asetil-KoA diangkut sebagai sitrat, yang sebelum ini telah terbentuk dalam matriks mitokondrion daripada asetil-KoA dan oksaloasetat. Tindak balas ini biasanya memulakan kitaran asid sitrik, tetapi apabila tidak memerlukan tenaga, ia diangkut ke sitoplasma, di mana ia dipecahkan kepada sitoplasma asetil-KoA dan oksaloasetat.
Satu lagi bahagian kitaran memerlukan NADPH bagi sintesis asid lemak.[4] Sebahagian kuasa penurunan ini dijana apabila oksaloasetat sitosol dikembalikan ke mitokondria selagi lapisan mitokondria dalaman tidak telap untuk oksaloasetat. Pertama, oksaloasetat dikurangkan kepada malat menggunakan NADH. Kemudian, malat dinyahkarboksilkan kepada piruvat. Kini, piruvat ini boleh memasuki mitokondrion dengan mudah, di mana ia dikarboksilkan semula kepada oksaloasetat oleh piruvat karboksilase. Dengan cara ini, pemindahan asetil-KoA daripada mitokondria ke dalam sitoplasma menghasilkan molekul NADH. Tindak balas keseluruhan yang bersifat spontan ini boleh diringkaskan sebagai:
- HCO3– + ATP + asetil-KoA → ADP + Pi + malonil-KoA
Sintesis asid amino
[sunting | sunting sumber]Enam asid amino penting dan tiga tidak penting disintesis daripada oksaloasetat dan piruvat.[5] Aspartat dan alanina terbentuk daripada oksaloasetat dan piruvat, masing-masing, melalui transaminasi glutamat. Asparagina disintesis dengan pengamidaan aspartat, dengan glutamin menderma NH4. Ini ialah asid amino tidak penting, dan laluan biosintetik ringkas ini wujud dalam semua organisma. Metionina, treonina, lisina, isoleusina, valina dan leusina ialah asid amino penting dalam manusia dan kebanyakan vertebrat. Laluan biosintetik mereka dalam bakteria adalah kompleks dan saling berkaitan.

Biosintesis oksalat
[sunting | sunting sumber]Oksaloasetat menghasilkan oksalat melalui hidrolisis.[6]
- oksaloasetat + H2 O ⇌ oksalat + asetat
Proses ini dimangkinkan oleh enzim oksaloasetase. Enzim ini wujud pada tumbuhan, tetapi tidak diketahui dalam haiwan.[7]
Rujukan
[sunting | sunting sumber]- ^ van Vugt-Lussenburg, BMA; van der Weel, L; Hagen, WR; Hagedoorn, P-L (February 26, 2021), "Biochemical Similarities and Differences between the Catalytic [4Fe-4S] Cluster Containing Fumarases FumA and FumB from Escherichia coli", PLOS ONE (diterbitkan February 6, 2013), 8 (2): e55549, doi:10.1371/journal.pone.0055549, PMC 3565967, PMID 23405168
- ^ M.V. Panchenko; A.D. Vinogradov (1991). "Direct demonstration of enol-oxaloacetate as an immediate product of malate oxidation by the mammalian succinate dehydrogenase". FEBS Letters. 286 (1–2): 76–78. doi:10.1016/0014-5793(91)80944-X. PMID 1864383.
- ^ "Welcome to The Chemistry Place". www.pearsonhighered.com. Dicapai pada 5 April 2018.
- ^ "fatty acids synthesis". www.rpi.edu.
- ^ "Animo acids synthesized from oxaloacetate and pyruvate". faculty.ksu.edu.sa. Diarkibkan daripada yang asal (PPTX) pada 2013-10-21. Dicapai pada 2013-10-21.
- ^ Gadd, Geoffrey M. "Fungal production of citric and oxalic acid: importance in metal speciation, physiology and biogeochemical processes" Advances in Microbial Physiology (1999), 41, 47-92.
- ^ Xu, Hua-Wei. "Oxalate accumulation and regulations is independent of glycolate oxidase in rice leaves" Journal of Experimental Botany, Vol 57, No. 9 pp. 1899-1908, 2006









