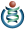Aedes aegypti
| Aedes aegypti | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

Larva de Aedes aegypti
| |||||||||||||||
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Aedes (Stegomyia) aegypti (Linnaeus, 1762) | |||||||||||||||
| Distribuição geográfica | |||||||||||||||
 | |||||||||||||||
| Sinónimos | |||||||||||||||
| Culex aegypti Linnaeus, 1762 Culex taeniatus Wiedemann, 1828 Culex excitans Walker, 1848 | |||||||||||||||
Aedes (Stegomyia) aegypti (aēdēs do grego αηδής: "odioso" e ægypti do latim, significando "do Egipto") é a nomenclatura taxonômica para o mosquito que é popularmente conhecido como mosquito-da-dengue ou pernilongo-rajado,[1] uma espécie de mosquito da família Culicidae proveniente da África, atualmente distribuído por quase todo o mundo, especialmente em regiões tropicais e subtropicais, sendo dependente da concentração humana no local para se estabelecer. Acredita-se que 35% da população mundial viva em áreas propícias e endêmicas para a proliferação do mosquito.[2]
O mosquito está bem adaptado à zonas urbanas, mais precisamente ao domicílio humano, onde consegue reproduzir-se e pôr os seus ovos em pequenas quantidades de água limpa e parada, isto é, pobres em matéria orgânica em decomposição e sais (que confeririam características ácidas à água), que preferivelmente estejam sombreados e no peridomicílio.
Atualmente, foi descoberto que a fêmea não se reproduz somente em água limpa e parada, pelo contrário. O mosquito pode se reproduzir em águas com altos níveis de poluição, como o esgoto por exemplo. A fêmea observa vários fatores influenciáveis ao crescimento das larvas, como a temperatura, luminosidade e resquícios de matéria orgânica. As larvas do aedes são sensíveis à luz, o que faz com que se desenvolvam bem em águas turvas.[3]
As fêmeas, para realizar a hematofagia, podem percorrer até 2 500 metros.[4] É considerado vector de doenças graves, como dengue, febre amarela, febre zica e chikungunya. O controle das suas populações é considerado assunto da saúde pública e há comprovação científica de que o controle do Aedes Aegypt tem custo menor para os governos do que o tratamento às doenças causadas por este vetor.[5]
Descrição
[editar | editar código-fonte]O Aedes aegypti é um mosquito que se encontra ativo e pica durante o dia, ao contrário do Anopheles, vector da malária, que tem atividade crepuscular. O Aedes aegypti tem, como vítima preferencial, o ser humano, e não faz praticamente som audível antes de picar. Mede menos de 1 centímetro e é preto com manchas brancas no corpo e nas pernas.[6]

O seu controle é difícil, por ser muito versátil na escolha dos criadouros onde deposita seus ovos, que são extremamente resistentes, podendo sobreviver vários meses até que a chegada de água propicie a incubação. Uma vez imersos, os ovos desenvolvem-se rapidamente em larvas, que dão origem às pupas, das quais surge o adulto. Como em quase todos os outros mosquitos, somente as fêmeas se alimentam de sangue para a maturação de seus ovos. Os machos se alimentam apenas de substâncias vegetais e açucaradas.[carece de fontes]
Por se adaptar bem a vários recipientes, a expansão deste mosquito a partir do seu habitat original foi rápida. O Aedes aegypti foi introduzido na América do Sul através de barcos provenientes de África. Nas Américas, admite-se que sua primeira colonização sobre o Novo Mundo ocorreu através dos navios negreiros no período colonial junto com os escravos. No Brasil, o Aedes aegypti havia sido erradicado na década de 1950; entretanto, nas décadas de 1960 e 1970, ele voltou a colonizar esse país, vindo de países vizinhos que não haviam conseguido promover a sua total erradicação.[carece de fontes]
O Aedes aegypti está presente nas regiões tropicais de África e da América do Sul, chegando à Ilha da Madeira, em Portugal e ao estado da Flórida, nos Estados Unidos. Nessa zona, o Aedes aegypti tem vindo a declinar, graças à competição com outra espécie do mesmo gênero, o Aedes albopictus. Este fato, porém, não trouxe boas notícias, uma vez que o A. albopictus é, também, um vetor da dengue, bem como de vários tipos de encefalite equina. No Brasil, o único que transmite a dengue é o A. aegypti. A competição entre as duas espécies ocorre devido ao fato de a fêmea do A. aegypti se acasalar tanto com o macho de sua espécie quanto com o macho do A. albopictus, que é mais agressivo e que, sendo de outra espécie, gera ovos inférteis, reduzindo, assim, a população de A. aegypti.[carece de fontes]O mosquito é tão proliferado que chega a infestar 3.592 municípios brasileiros.[2]
Repelentes baseados no composto DEET (N,N-dietilmetatoluamida) são recomendados contra o Aedes aegypti.[7][8]
Genoma
[editar | editar código-fonte]
O genoma desta espécie de mosquito foi sequenciado e analisado por um consórcio que inclui cientistas do Instituto J. Craig Venter, do Instituto Europeu de Bioinformática, do Instituto Broad e da Universidade de Notre Dame, e foi publicado em 2007. O esforço de sequenciamento de seu DNA foi destinado a fornecer novos caminhos para pesquisas em inseticidas, bem como para possíveis alterações genéticas que impeçam a propagação dos vírus levados pelo inseto.[9]
Esta foi a segunda espécie de mosquito que teve seu genoma sequenciado integralmente (o primeiro foi o Anopheles gambiae). Os dados publicados incluem 1380 milhões de pares de bases contendo cerca de 15 419 genes que codificam proteínas do mosquito. A sequência indica que a espécie divergiu da Drosophila melanogaster (mosca-comum-da-fruta) há cerca de 250 milhões de anos, enquanto o Anopheles gambiae divergiu de D. melanogaster há cerca de 150 milhões de anos.[10]
Formas de controle
[editar | editar código-fonte]Mecânico
[editar | editar código-fonte]

Baseia-se na eliminação de possíveis locais de incubação dos ovos do mosquito, ou seja, na eliminação de locais de água parada.[11] Outra forma de controle mecânico são as armadilhas adesivas de ovoposição (BR-OVT), que atraem os mosquitos adultos graças a sua forma, cor e, em alguns casos, pela presença de feromônios. Além de prenderem os insetos na sua borda adesiva, as armadilhas induzem as fêmeas a depositarem seus ovos em uma substância larvicida (BTi).[12]
Biológico
[editar | editar código-fonte]Consiste na utilização de algumas espécies que combatem o mosquito, como algumas espécies de peixes e microcrustáceos que se alimentam das larvas do inseto, por exemplo.[11] Bactérias do gênero Wolbachia também podem ser usadas, pois infectam o inseto e o tornam imunes aos vírus usualmente transmitidos pelo inseto. A bactéria Bacillus thuringiensis israelensis (BTi) é patogênica para o inseto, pois produz toxinas que geram poros no intestino do inseto. Esta toxina pode ser produzida em laboratório e utilizada na produção de larvicidas.[12] A Crotalaria juncea também é utilizada, pois é uma planta que atrai as libélulas, que costumam se alimentar dos adultos e das larvas de A. aegypti.[13]
Químico
[editar | editar código-fonte]Baseia-se no uso de inseticidas, que atacam a larva ou a forma adulta do inseto. Os inseticidas mais comuns são compostos, como os piretroides, os organofosforados e os carbamatos. Eles interferem no sistema nervoso do inseto, causando sua superexcitação ou inibição. São os mesmos compostos utilizados nos agrotóxicos e, portanto, são tóxicos também para outras espécies, inclusive para o ser humano, e podem ter um efeito cumulativo ao longo da cadeia alimentar. Outro problema é que o uso de inseticidas pode acabar gerando insetos resistentes.[12] Um exemplo de controle químico é o fumacê, que ataca a forma adulta do inseto. Porém a forma mais eficiente de controle químico é o que combate as larvas do inseto, por estas estarem em locais mais restritos do que os insetos adultos, que voam.[11]
Para amenizar tais adversidades, foram desenvolvidos outros produtos para fazer o controle desses vetores e são, principalmente, os grupos dos inseticidas biológicos ( ex: bactérias patógenas) e dos reguladores de crescimento.[14]
Monitoramento
[editar | editar código-fonte]O Monitoramento Integrado do Aedes (MI-Aedes) é uma tecnologia brasileira resultante do desenvolvimento de pesquisas sobre a biologia e comportamento do mosquito, com o objetivo de monitorar o vetor e a circulação viral em área urbana. Criada em 2002, a partir da formalização de uma empresa spin-off acadêmica com origem no Instituto de Ciências Biológicas da Universidade Federal de Minas Gerais (UFMG), a empresa licenciou suas primeiras tecnologias da UFMG em 2004, por meio do financiamento público da Financiadora de Estudos e Projetos (FINEP), Fundo Verde-Amarelo para o desenvolvimento tecnológico. Desde então a empresa, em 2010, juntamente com a Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG) e a própria UFMG, desenvolveu a tecnologia de monitoramento integrado (MI-Aedes) de diferentes vírus em mosquitos, hoje responsável pelo único monitoramento de dengue, zika e chikungunya em vetores.[15]
Genético
[editar | editar código-fonte]A. aegypti geneticamente modificados, apelidados de Aedes aegypti do bem,[12] foram criados para suprimir a sua própria espécie, em uma abordagem semelhante à técnica do inseto estéril, reduzindo, assim, o risco de propagação de doenças. Os mosquitos, conhecidos como OX513A, foram desenvolvidos pela empresa Oxitec, Universidade de Oxford e subsidiária da Intrexon (NYSE: XON). Os testes de campo nas Ilhas Cayman, Brasil e Panamá têm mostrado que os mosquitos OX513A reduziram as populações de mosquitos alvo em mais de 90%.[16][17]

O efeito de supressão da população do inseto é conseguido através um gene autolimitador que impede que a prole sobreviva. Mosquitos geneticamente modificados do sexo masculino, que não picam ou transmitem doenças, são liberados para acasalar com as fêmeas selvagens. Sua prole, então, herda o gene autolimitador e morre antes de atingir a idade adulta, ou seja, antes que possam se reproduzir ou espalhar doenças. Os mosquitos OX513A e seus descendentes também carregam um marcador fluorescente para monitoramento. Para produzir mais mosquitos OX513A para projetos de controle, o gene autolimitador é desligado na instalação de produção de mosquito usando um antídoto (o antibiótico tetraciclina), o que permite que os mosquitos voltem a se reproduzir naturalmente. No meio ambiente, este antídoto não está disponível e, assim, a população da praga é suprimida.[18]
Os efeitos desta técnica não são tóxicos e os espécimes geneticamente modificados cruzam com outros Ae. aegypti. Os insetos libertados e seus descendentes morrem e não persistem no ambiente.[19][20]
No Brasil, os mosquitos geneticamente modificados foram aprovados pela Comissão Técnica Nacional de Biossegurança (CTNBio) para lançamentos em todo o país. O município de Piracicaba, no interior de São Paulo, lidera a primeira parceria do mundo para a liberação de mosquitos OX513A.[21][22] Com os resultados, a Câmara dos Lordes, do Parlamento do Reino Unido, apelou para que o governo britânico apoie mais pesquisas sobre insetos geneticamente modificados para a saúde global.[23]
Esta abordagem também pode ser aplicada para controlar o Aedes albopictus e os mosquitos Anopheles, que propagam o paludismo.[24]
Mosquitos geneticamente modificados (GM) criado pela empresa Oxitec e soltos em Jacobina, entre 2013 e 2015, entre 5% e 60% da população de mosquitos carregava DNA da linhagem Oxitec em seu genoma em diferentes pontos de um estudo e em diferentes bairros de Jacobina. Um artigo publicado no Scientific Reports[25] sugere que o DNA da cepa Oxitec poderia tornar os mosquitos selvagens mais aptos ou mais fortes. Dra. Capurro apontou que não havia dados que sustentassem a ideia de "vigor híbrido".[26] A Oxitec reagiu à publicação do artigo com uma lista de objeções e registrou uma queixa com a revista Scientific Reports.[27] A empresa realizou vários testes no Brasil desde a libertação em Jacobina, incluindo um teste de uma cepa GM de segunda geração[28] projetada para que os filhotes sobrevivam e transmitam seus genes.[29]
Ver também
[editar | editar código-fonte]Referências
- ↑ FERREIRA, A. B. H. Novo Dicionário da Língua Portuguesa. Segunda edição. Rio de Janeiro: Nova Fronteira, 1986. p.1 314
- ↑ a b Nunes, Jordana Guimarães (2015). «Chikungunya e Dengue: Desafio para a saúde pública no Brasil». Universidade Estadual de Goiás
- ↑ «Cuidado, o Aedes aegypti também consegue se reproduzir em água suja». Época. Consultado em 22 de março de 2016
- ↑ NEVES.David Pereira. et. al'.' Parasitologia Humana. 10.ed. São Paulo: Atheneu, 2000.
- ↑ «Kantar - Combate ao Aedes aegypti custa menos que tratamentos de dengue, zika, febre amarela e chikungunya». br.kantar.com. Consultado em 5 de outubro de 2017
- ↑ «Aprenda a reconhecer o mosquito Aedes aegypti». Prefeitura da cidade de São Paulo. Consultado em 19 de outubro de 2012. Arquivado do original em 21 de junho de 2012
- ↑ Governo do Estado do Rio de Janeiro, Rio Contra Dengue, Tire suas dúvidas [em linha]
- ↑ Prefeitura de Santos, SP, Dengue, Transmissão [em linha]
- ↑ Heather Kowalski (17 de maio de 2007). «Scientists at J. Craig Venter Institute publish draft genome sequence from Aedes aegypti, mosquito responsible for yellow fever, dengue fever». J. Craig Venter Institute
- ↑ Vishvanath Nene, Jennifer R. Wortman, Daniel Lawson, Brian Haas, Chinnappa Kodira; et al. (Junho de 2007). «Genome sequence of Aedes aegypti, a major arbovirus vector». Science. 316 (5832): 1718–1723. Bibcode:2007Sci...316.1718N. PMC 2868357
 . PMID 17510324. doi:10.1126/science.1138878
. PMID 17510324. doi:10.1126/science.1138878
- ↑ a b c Aedes aegypti. Disponível em http://auladengue.ioc.fiocruz.br/?p=86. Acesso em 7 de julho de 2016.
- ↑ a b c d Instituto do Cérebro. Disponível em http://inscer.pucrs.br/artigo-controle-do-mosquito-aedes-aegypti-profa-dra-celia-carlini-pesquisadora-da-area-de-biologia-celular-e-molecular-no-inscer/. Acesso em 7 de julho de 2016.
- ↑ Livre pensar é só pensarǃ. Disponível em https://livrepensar.wordpress.com/?s=beleza+para+combater+o+mosquito. Acesso em 7 de julho de 2016.
- ↑ Braga, Ima Aparecida; Valle, Denise (2007). «Aedes aegypti: inseticidas, mecanismos de ação e resistência». Epidemiol. Serv. Saúde. v. 16 (n. 4): 179-293. Consultado em 30 de abril de 2018
- ↑ «Ecovec». ecovec.com. Consultado em 4 de setembro de 2017
- ↑ Danilo O. Carvalho, Andrew R. McKemey, Luiza Garziera, Renaud Lacroix, Christl A. Donnelly, Luke Alphey, Aldo Malavasi, Margareth L. Capurro (julho de 2015). «Suppression of a Field Population of Aedes aegypti in Brazil by Sustained Release of Transgenic Male Mosquitoes». PLOS Neglected Tropical Diseases: 1–15. doi:10.1371/journal.pntd.0003864
- ↑ Kate Kelland (16 de dezembro de 2015). «Lawmakers call for British trials of genetically modified insects». Reuters. Consultado em 16 de dezembro de 2015
- ↑ Zoe Curtis, Kelly Matzen, Marco Neira Oviedo, Derric Nimmo, Pamela Gray, Peter Winskill, Marco A. F. Locatelli, Wilson F. Jardim, Simon Warner, Luke Alphey, Camilla Beech (agosto de 2015). «Assessment of the Impact of Potential Tetracycline Exposure on the Phenotype of Aedes aegypti OX513A: Implications for Field Use». PLOS Neglected Tropical Diseases: 1–15. doi:10.1371/journal.pntd.0003999
- ↑ Kevin Gorman, Josué Young, Lleysa Pineda, Ricardo Márquez, Nestor Sosa, Damaris Bernal, Rolando Torres, Yamilitzel Soto, Renaud Lacroix, Neil Naish, Paul Kaiser, Karla Tepedino, Gwilym Philips, Cecilia Kosmann, Lorenzo Cáceres (setembro de 2015). «Short-term suppression of Aedes aegypti using genetic control does not facilitate Aedes albopictus». Pest Management Science. doi:10.1002/ps.4151
- ↑ Oreenaiza Nordin, Wesley Donald, Wong Hong Ming, Teoh Guat Ney, Khairul Asuad Mohamed, Nor Azlina Abdul Halim, Peter Winskill, Azahari Abdul Hadi, Zulkamal Safi'in Muhammad, Renaud Lacroix, Sarah Scaife, Andrew Robert McKemey, Camilla Beech, Murad Shahnaz, Luke Alphey, Derric David Nimmo , Wasi Ahmed Nazni, Han Lim Lee (março de 2013). «Oral Ingestion of Transgenic RIDL Ae. aegypti Larvae Has No Negative Effect on Two Predator Toxorhynchites Species». PLOS One. 8 (3): 1–7. doi:10.1371/journal.pone.0058805
- ↑ Justine Alford via IFLScience (25 de julho de 2014). «Brazil To Unleash Genetically Modified Mosquitoes». Huffington Post. Consultado em 25 de julho de 2014
- ↑ no by-line (30 de abril de 2015). «Modified mosquitoes enter the war against dengue in São Paulo». G1. Consultado em 30 de abril de 2015
- ↑ «Release potential of GM insects to fight disease and pests». House of Lords Science and Technology Select Committee / Parliament UK. 17 de dezembro de 2015. Consultado em 17 de dezembro de 2015
- ↑ «Release potential of GM insects to fight disease and pests». House of Lords Science and Technology Select Committee / Parliament UK. 17 de dezembro de 2015. Consultado em 17 de dezembro de 2015
- ↑ Evans, Benjamin R.; Kotsakiozi, Panayiota; Costa-da-Silva, Andre Luis; Ioshino, Rafaella Sayuri; Garziera, Luiza; Pedrosa, Michele C.; Malavasi, Aldo; Virginio, Jair F.; Capurro, Margareth L. (10 de setembro de 2019). «Transgenic Aedes aegypti Mosquitoes Transfer Genes into a Natural Population». Scientific Reports (em inglês). 9 (1): 1–6. ISSN 2045-2322. doi:10.1038/s41598-019-49660-6
- ↑ «Brazilian author asks for retraction of Oxitec mosquito paper». QC. Consultado em 2 de outubro de 2019
- ↑ «Oxitec responds to article entitled 'Transgenic Aedes aegypti Mosquitoes Transfer Genes into a Natural Population'». Oxitec (em inglês). Consultado em 2 de outubro de 2019
- ↑ «Oxitec Successfully Completes First Field Deployment of 2nd Generation Friendly Aedes aegypti Technology». Oxitec (em inglês). Consultado em 2 de outubro de 2019
- ↑ ServickOct. 1, Kelly; 2019; Pm, 1:00 (1 de outubro de 2019). «Dissent splits authors of provocative transgenic mosquito study». Science | AAAS (em inglês). Consultado em 2 de outubro de 2019
Bibliografia
[editar | editar código-fonte]- Consoli RAGB, Lourenço-de-Oliveira R. Principais mosquitos de importância sanitária no Brasil. Editora Fundação Instituto Oswaldo Cruz, Rio de Janeiro, Brasil, 1994.
- Forattini OP. Culicidologia médica: identificação, biologia, epidemiologia v.2. EDUSP São Paulo, 2002.
Ligações externas
[editar | editar código-fonte]- Moderno Sistema de Geoprocessamento- COPPE/UFRJ e UECE. O sistema permite ao gestor acompanhar em tempo real o trabalho do controles de vetores e da rede hospitalar.
- «Catálogo de mosquitos»
- «Rio Contra Dengue» Site com dicas de prevenção, informações sobre tratamento e notícias sobre o combate à dengue no Rio de janeiro.