Kalia bisulfato
Aspekto
| Kalia bisulfato | |||
 | |||
| Plata kemia strukturo de la Kalia bisulfato | |||
 | |||
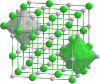
| Tridimensia kemia strukturo de la Kalia bisulfato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 7646-93-7 | ||
| ChemSpider kodo | 56396 | ||
| PubChem-kodo | 516920 | ||
| Merck Index | 15,7734 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora senodora solidaĵo | ||
| Molmaso | 136.162 g·mol−1 | ||
| Denseco | 2.245g cm−3 | ||
| Fandpunkto | 197 °C | ||
| Bolpunkto | 300 °C | ||
| Acideco (pKa) | 1.92 | ||
| Solvebleco | Akvo:366 g/L | ||
| Mortiga dozo (LD50) | 2340 mg/kg (buŝe)[1] | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H314, H318, H335[2] | ||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P271, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P312, P321, P363, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Kalia bisulfato aŭ kalia hidrogensulfato (kun la kemia formulo KHSO4) estas neorganika komponaĵo, blanka, likveska solidaĵo kun iomete sulfura odoro, kalia salo de la hidrogeno-sulfata acido aŭ bisulfata acido. Merkalito, la erco enhavanta kalian bisulfaton estas rare trovata. Ĝi uzatas kiel laksigilo en medicino. Ĉar ĝi estas solvebla en akvo, ĝiaj solvaĵoj estas acidaj kaj korodaj. Ĝi estas toksa substanco kiam ingestita aŭ per haŭtokontakto. Per termolizo ĝi malkomponiĝas en pirosulfaton.
Sintezo
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Kalia bisulfato estas preparata per agado de la kalia hidroksido sur sulfata acido:
Sintezo 2
[redakti | redakti fonton]- Kalia bisulfato estas preparebla per interagado de la kalia sulfato kaj sulfata acido:
Sintezo 3
[redakti | redakti fonton]- Kalia bisulfato estas preparata per agado de la kalia klorido sur sulfata acido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]Bisulfatoj donas sulfatojn kiam varmigitaj:
Reakcio 2
[redakti | redakti fonton]Bisulfatoj donas pirosulfatojn ĉe pli altaj temperaturoj:
Reakcio 3
[redakti | redakti fonton]Kalia bisulfato iĝas en kalia sulfato kiam fandiĝas kun kalia hidroksido:
Reakcio 4
[redakti | redakti fonton]- Bisulfato de kalio fandiĝas kun kalia klorido estigante kalian sulfaton kaj HCl:
Reakcio 5
[redakti | redakti fonton]Kiam fanditaj, kelkaj nesolveblaj oksidoj iĝas en solveblaj komponaĵoj:
Literaturo
[redakti | redakti fonton]- ThermoFisher Arkivigite je 2017-08-24 per la retarkivo Wayback Machine
- LabChem Arkivigite je 2017-08-24 per la retarkivo Wayback Machine
- Merck Millipore
- Chemical Book
- Analytical Methods for a Textile Laboratory, J. William Weaver
- Handbook of Preservatives, Michael Ash
- Academic Press Dictionary of Science and Technology, Christopher G. Morris, Academic Press
Vidu ankaŭ
[redakti | redakti fonton]Referencoj
[redakti | redakti fonton]- ↑ Science Laboratories. Arkivita el la originalo je 2017-09-09. Alirita 2017-08-24 .
- ↑ Pubchem
| ||||||